��Ŀ����
������ȫ������װ�е������ƣ�NaN3���ȹ����ĩ����ҵ�Ͻ�����������ˮ��Һ����NH3����Ӧ�ð����ƣ�NaNH2�����ٽ���������һ����������Ӧ�����ɵ������ơ��������ƺͰ���������˵���У�����ȷ���ǣ� ��
| A����ȫ������ѡ�õ������Ƶ�ԭ�������NaN3Ѹ�ٷֽ�ų�����N2 |
| B���ƿ�����ˮ��Ӧ |
C���Ʊ��������Ʒ�Ӧ�У���Ҫ�漰�Ļ�ѧ����ʽΪ��Na+NH3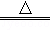 NaNH2+H2�� 2NaNH2+N2O NaNH2+H2�� 2NaNH2+N2O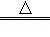 NaN3+NaOH+NH3�� NaN3+NaOH+NH3�� |
| D����ҵ��NaN3�п��ܺ���Na2CO3 |
C
���������A����ѧ��Ӧǰ��Ԫ������䣬��ȫ������ѡ�õ������Ƶ�ԭ�������NaN3Ѹ�ٷֽ�ų�����N2����ȷ��B�����ݹ�ҵ�Ͻ�����������ˮ��Һ����NH3����Ӧ�ð����ƣ�NaNH2�������е�Һ�����п�֪���ƿ�����ˮ��Ӧ����ȷ��C���Ʊ��������Ʒ�Ӧ�У���Ҫ�漰�Ļ�ѧ����ʽΪ��2Na+2NH3
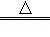 2NaNH2+H2�� 2NaNH2+N2O
2NaNH2+H2�� 2NaNH2+N2O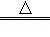 NaN3+NaOH+NH3����C�е�һ����ѧ����ʽû��ƽ���ʴ���D����ҵ��NaN3�п��ܺ���Na2CO3����ȷ��
NaN3+NaOH+NH3����C�е�һ����ѧ����ʽû��ƽ���ʴ���D����ҵ��NaN3�п��ܺ���Na2CO3����ȷ��
��ϰ��ϵ�д�
 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�
�����Ŀ
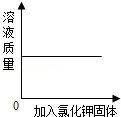 B��
B��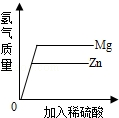
 D��
D��