题目内容
现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液。为了测定碱性调味液中碳酸钠的质量分数,某同学进行了如下实验:取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某浓度的稀硫酸中,测得三组实验数据见下表(气体的溶解忽略不计):
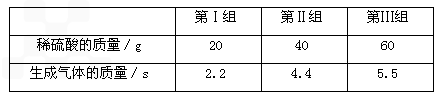
根据实验及有关数据进行计算:
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为 ___________g。
(2)碱性调味液中碳酸钠的质量分数为多少?
(3)100g碱性调味液与该稀硫酸反应后溶液pH=7时,消耗稀硫酸的质量为多少克?
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为 ___________g。
(2)碱性调味液中碳酸钠的质量分数为多少?
(3)100g碱性调味液与该稀硫酸反应后溶液pH=7时,消耗稀硫酸的质量为多少克?
(1)5.5g
(2)解:设碱性调味液中碳酸钠的质量为x
Na2CO3 + H2SO4==== Na2SO4 + CO2↑ + H2O
106 44
x 5.5g
106:44 = x:5.5g ,x=12.25g
12.25g/100g×100%=12.25%
(3) 设反应后溶液pH=7时需要稀硫酸的质量为y
2.2g:20g=5.5g:y , y=50g
答:(2)碱性调味液中碳酸钠的质量分数为12.25%;
(3)反应后溶液pH=7时,需要稀硫酸的质量为50g。
(2)解:设碱性调味液中碳酸钠的质量为x
Na2CO3 + H2SO4==== Na2SO4 + CO2↑ + H2O
106 44
x 5.5g
106:44 = x:5.5g ,x=12.25g
12.25g/100g×100%=12.25%
(3) 设反应后溶液pH=7时需要稀硫酸的质量为y
2.2g:20g=5.5g:y , y=50g
答:(2)碱性调味液中碳酸钠的质量分数为12.25%;
(3)反应后溶液pH=7时,需要稀硫酸的质量为50g。

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液.为了测定碱性调味液中碳酸钠的质量分数,某同学进行了如下实验:取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某浓度的稀硫酸中,测得三组实验数据见下表(气体的溶解忽略不计):
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀硫酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/s | 2.2 | 4.4 | 5.5 |
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为______g.
(2)碱性调味液中碳酸钠的质量分数为多少?
(3)100g碱性调味液与该稀硫酸反应后溶液pH=7时,消耗稀硫酸的质量为多少克?
 (2011?佛山)现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液.为了测定碱性调味液中碳酸钠和氯化钠的质量分数,设计了如下实验方案.
(2011?佛山)现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液.为了测定碱性调味液中碳酸钠和氯化钠的质量分数,设计了如下实验方案.