题目内容
含镁3%-5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为W g的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.
[查阅资料]已知铝与NaOH溶液反应生成易溶于水的偏铝酸钠(NaAlO2)和H2,化学方程式为:2A1+2NaOH+2H2O=2NaAlO2+3H2↑;镁不与NaOH溶液反应.氢氧化铝能与氢氧化钠溶液发生反应生成易溶于水的偏铝酸钠(NaAlO2)和H2O,化学方程式为:A1(OH)3+NaOH=NaAlO2+2H2O;氢氧化镁不与氢氧化钠溶液反应.
[提出猜想]利用镁铝与酸、铝与碱、氢氧化铝与碱反应的化学性质来测定合金中镁的质量分数.
[设计方案]研究小组设计了不同的实验方案.
方案l:镁铝合金与过量盐酸反应测定生成气体在标准状况下的体积为V0L;
方案2:镁铝合金与过量NaOH溶液充分反应后,过滤、洗涤、干燥、称量剩余固体的质量为W1g;
方案3:镁铝合金与过量盐酸溶液反应后再与过量NaOH溶液反应,过滤、洗涤、干燥、称量沉淀的质量为W2g.
[问题讨论]请你参与研究小组的研究过程,并回答有关问题:
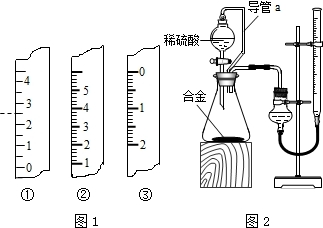
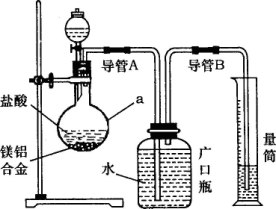
(1)研究小组利用上图所示实验装置,按照方案1进行了实验.
①装置中仪器a的名称是________.
②实验装置中有一处明显错误,请指出________
(2)方案2中剩余固体是________;若按方案2进行实验,测得镁的质量分数为________.
(3)方案3中“过滤”得到的沉淀是________.
(4)某同学又设计了与上述方案原理不同的方案4,也能测得镁的质量分数.请你在横线上填写合适的内容,将该方案补充完整.
方案4:镁铝合金与________反应测定生成气体在标准状况下的体积为V2L.
[方案评价]
(5)在实验方案1-4中,你认为最佳的实验方案是________.
解析:
|
(1)①圆底烧瓶(1分);②广口瓶中进气导管插入水中;排水导管未插至广口瓶底部(2分) (2)Mg或镁(2分),詈×l00%(1分) (3)Mg(OH)2或氢氧化镁(2分) (4)过量NaOH溶液(1分) (5)方案2(1分) |

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案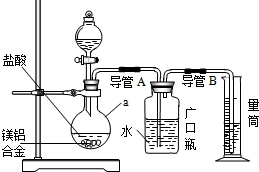 含镁3%一5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为W 9的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.
含镁3%一5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为W 9的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.