题目内容
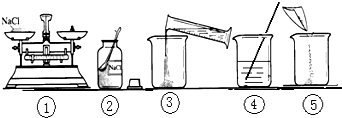
在实验室配制100g 10%的氯化铵溶液并探究酸碱性强弱与浓度及温度的关系.请回答有关问题:
①计算:需氯化铵的质量 g,水 mL;
②称量:用电子天平称取所需的氯化铵,用 (选填“50mL”、“100mL”或“200mL”)的量筒量取所需水的体积;
③溶解:将上述称量好的氯化铵和水放到烧杯中,用玻璃棒搅拌,其作用是 .
④反思:若称取的氯化铵中含有水分或其它杂质,则所配制的氯化铵溶液的溶质质量分数会 .(选填“偏大”、“不变”或“偏小”)
⑤测溶液的酸碱性:用pH试纸测得氯化铵溶液的pH为5,则其为 性.为进一步探究其酸碱性的强弱与溶液的浓度、温度是否有关,采用以下四个步骤研究.请完成第二、第三步实验步骤. (不必写实验中涉及的仪器)
第一步:分别配制溶质质量分数为5%、10%、20%的氯化铵溶液;
第二步:在相同 下;分别测5%、10%、20%的氯化铵溶液的pH;
第三步: ;
第四步:根据测得数据,综合分析得出氯化铵溶液酸碱性的强弱与浓度、温度关系.
①计算:需氯化铵的质量
②称量:用电子天平称取所需的氯化铵,用
③溶解:将上述称量好的氯化铵和水放到烧杯中,用玻璃棒搅拌,其作用是
④反思:若称取的氯化铵中含有水分或其它杂质,则所配制的氯化铵溶液的溶质质量分数会
⑤测溶液的酸碱性:用pH试纸测得氯化铵溶液的pH为5,则其为
第一步:分别配制溶质质量分数为5%、10%、20%的氯化铵溶液;
第二步:在相同
第三步:
第四步:根据测得数据,综合分析得出氯化铵溶液酸碱性的强弱与浓度、温度关系.
分析:根据配制一定质量分数溶液的步骤:计算、称量、溶解,及所需注意事项来解答①③④,因为是测定溶液在温度与浓度对pH的影响,因此应先创设设置温度不同浓度相同的条件,而后在温度相同不同浓度的条件进行对比实验来解答⑤.
解答:解:①计算:氯化铵的质量=溶液质量×溶质的质量分数=100g×10%=10g,水的质量=100g-10g=90g,水的体积为:90g÷1g/mL=90mL;
②称量:用托盘天平称取所需的氯化铵;溶解:水的体积为:90g÷1g/mL=90mL,量筒规格为100mL;
③溶解时,玻璃棒的作用是加快溶解;
④若称取的氯化铵中含有水分,导致实际称取的氯化铵质量小于应该称取的质量,则溶质质量减小,所配制的溶液的质量分数偏小;
⑤创设对比实验的前提就是控制相同条件下不同的项目的比较,即定溶液状态或定温状态下进行.用pH试纸测得氯化铵溶液的pH为5,小于7,则其为酸性.
第二步:同温条件下,测定不同浓度溶液的pH;
第三步:测定某一浓度溶液在不同温度时的pH.
故答案为:①10;90;
②100mL;
③加速溶解;
④偏小;
⑤酸;温度;分别测10%的氯化铵溶液在不同温度下的pH.
②称量:用托盘天平称取所需的氯化铵;溶解:水的体积为:90g÷1g/mL=90mL,量筒规格为100mL;
③溶解时,玻璃棒的作用是加快溶解;
④若称取的氯化铵中含有水分,导致实际称取的氯化铵质量小于应该称取的质量,则溶质质量减小,所配制的溶液的质量分数偏小;
⑤创设对比实验的前提就是控制相同条件下不同的项目的比较,即定溶液状态或定温状态下进行.用pH试纸测得氯化铵溶液的pH为5,小于7,则其为酸性.
第二步:同温条件下,测定不同浓度溶液的pH;
第三步:测定某一浓度溶液在不同温度时的pH.
故答案为:①10;90;
②100mL;
③加速溶解;
④偏小;
⑤酸;温度;分别测10%的氯化铵溶液在不同温度下的pH.
点评:此题考查一定溶质质量分数溶液的配制和探究酸碱性的强弱与其浓度及温度的关系,解题的关键是对PH试纸的使用,以及对比实验的设计.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目