��Ŀ����
����Ŀ��ˮ��һ����Ҫ����Ȼ��Դ��
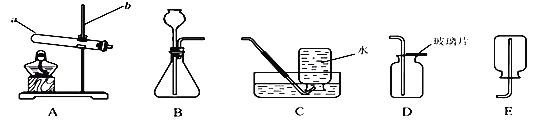
(1)ͨ�����ˮ��ʵ�飬��֪ˮ��________��ɡ���Ӧ�Ļ�ѧ����ʽΪ_____________��
(2)С������ͼ��ʾ�ļ���ˮ��������ˮ��Ʒ��
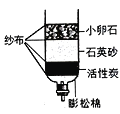
ͼ�л���̿�ɳ�ȥˮ�е�ɫ�غ���ζ����Ϊ���������õ�__________�ԣ�С�����������ˮ�м���_________�����ֲ�������ĭ���٣������γɽ϶״��϶��ú�ˮΪӲˮ��
(3)Ӳˮ����������������ܶ��鷳�������п���_______________�ķ���������ˮ��Ӳ�ȣ�
(4)����ˮ�������û�֮ǰ��������ɱ������������ˮ������ClO2�������·�Ӧ�Ʊ�: C12 + 2NaC1O2 = 2X+ 2C1O2,X�Ļ�ѧʽΪ_____________��
���𰸡� ��Ԫ�غ���Ԫ�� 2H2O![]() 2H2��+O2�� ���� ����ˮ ������� NaCl
2H2��+O2�� ���� ����ˮ ������� NaCl
����������1�����ˮ��������������������������Ԫ����ɵģ�����������Ԫ����ɵģ���ˮ������Ԫ�غ���Ԫ����ɵģ���ѧ����ʽΪ��2H2O![]() 2H2��+O2����
2H2��+O2����
��2������̿�������õ������ԣ�����װ�ô�������ˮ�У�������������ˮ�������а�ɫ��״�������˵����Ӳˮ��
��3�������У�������еķ���������ˮ��Ӳ����
��4���������غ㶨�ɣ���Ӧǰ��ԭ�����ࡢ��Ŀ�����䣬�ɷ�Ӧ�Ļ�ѧ����ʽCl2+2NaClO2�T2X+2ClO2����Ӧǰ�ȡ��ơ���ԭ�Ӹ����ֱ�Ϊ4��2��4����Ӧ������������ȡ��ơ���ԭ�Ӹ����ֱ�Ϊ2��0��4�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��2X�����к���2����ԭ�ӡ�2����ԭ�ӣ���ÿ��X������1����ԭ�ӡ�1����ԭ�ӹ��ɣ�������X�Ļ�ѧʽΪNaCl��

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�����Ŀ�������� KCl�IJ����ܽ�����ݣ�����˵������ȷ����( )
�¶ȣ��棩 | 0 | 20 | 40 | 60 |
�ܽ�ȣ�g/100gˮ�� | 27.6 | 34.0 | 40.0 | 45.5 |
A.KCl������Һ�в������ܽ���������
B.20��ʱ��100g KCl������Һ�к�KCl 34.0 g
C.20���KCl��Һ��Ũ��һ��С�� 40���KCl������Һ��Ũ��
D.60��ʱ����һ����������KCl��Һ���µ�40�棬һ���о�������