题目内容
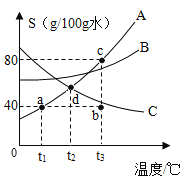
【题目】下图为四种物质的溶解度曲线。则下列说法错误的是
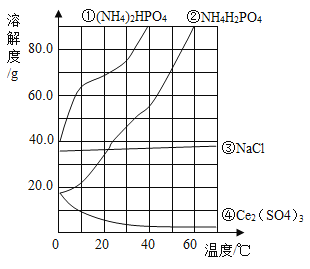
A.当温度为10℃时,物质溶解度关系为①>③>②>④
B.若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶
C.在l0℃时把NH4H2PO4和Ce2(SO4)3的饱和溶液升温到30℃ ,有晶体析出的是Ce2(SO4)3
D.22℃时(NH4)2HPO4饱和溶液的质量分数约为70%
【答案】D
【解析】A.在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。当温度为10℃时,物质溶解度关系为①>③>②>④; B.若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶,磷酸二氢铵因溶解度迅速减小而析出,氯化钠的溶解度受温度很小,氯化钠的量又少,所不析出,过滤可得较纯净的磷酸二氢铵;C.在l0℃时把NH4H2PO4和Ce2(SO4)3的饱和溶液升温到30℃ ,Ce2(SO4)3因溶解度变小,有晶体析出,NH4H2PO4的溶解度增大,变成不饱和溶液,不析出晶体;D.溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% 。22℃时(NH4)2HPO4饱和溶液的质量分数小于70%;选D

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】对空气中氧气含量测定的再认识。
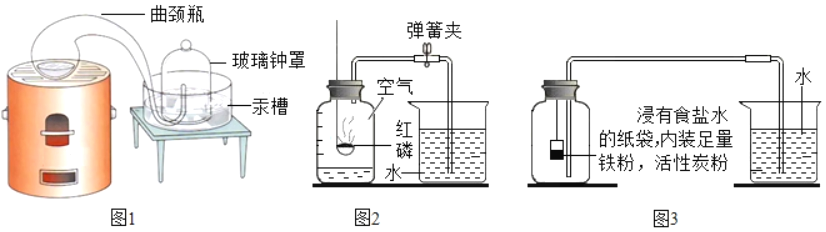
(经典赏析)用图1装置测定空气中氧气含量的科学家是_____。
(1)该实验中选择汞为实验药品,把它放在密闭的容器里连续加热12天,发现一部分银白色的液态汞变成红色粉末,同时容器里空气的体积差不多减少![]() ,对应观察到的现象为_____。
,对应观察到的现象为_____。
(2)该实验中使用汞的缺点是_____。
A 汞有毒,实验过程中不安全 B 汞为液态,在汞槽中起到液封作用
C 生成的化合物加热分解又能得到汞和氧气 D 实验时间太长
(实验回顾)图2是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的文字表达式:_____。
(2)实验原理:由于红磷燃烧消耗空气中氧气,使瓶内减小,烧杯中水倒吸到集气瓶中。用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
(3)对该实验认识正确的是_____。
A 红磷燃烧产生大量白色的烟雾
B 红磷的用量不足会导致测定氧气体积含量偏大
C 红磷燃烧以后,须冷却到室温方可打开止水夹
D 该实验可说明氮气难溶于水
(问题提出)某小组同学多次实验发现,集气瓶内上升的水面始终小于理论值。经查阅资料知:
燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测得结果与理论值相差较大。
(实验改进)Ⅰ.根据铁丝在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图3实验装置,再次测定空气中氧气含量,装置中的食盐水和活性炭会加速铁生锈。
Ⅱ.测得实验数据如表:
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(1)根据表中数据计算,改进实验后测得的空气中氧气体积分数是_____。(消耗的水的体积忽略不计,计算结果精确到0.1%)。
(2)实验反思:从原理的角度分析,与红磷燃烧法相比,用铁丝生锈法测定空气中氧气含量的优点是_____。
(经典再识)科学家选择汞作为药品也有优点:汞的沸点为356.6℃,加热时源源不断气化的汞原子和空气中的氧分子发生的反应属于气相反应,反应可以达到完全,因此汞_____(填“能”或“不能”)将密闭容器内的氧气几乎耗尽!