��Ŀ����
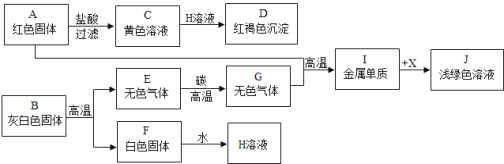
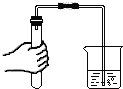
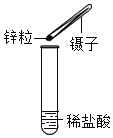
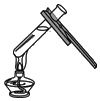
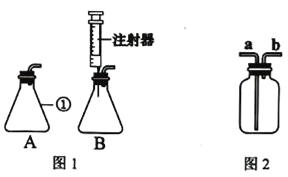
����Ŀ��ʵ������ȡ����ʱһ��������ػ������ػ����������Һ����ȡ��������ͼ�����õ�ʵ��װ�ã�
 (1)ʵ���Ҳ��÷ֽ����������Һ��ȡ����ʱ��Ҫ���Ʊ����ռ�װ��Ϊ____��(���ţ���ͬ)���÷�Ӧ�û�ѧ����ʽΪ____������Fװ�����ռ�������������________��ͨ��(����a������b��)��
(1)ʵ���Ҳ��÷ֽ����������Һ��ȡ����ʱ��Ҫ���Ʊ����ռ�װ��Ϊ____��(���ţ���ͬ)���÷�Ӧ�û�ѧ����ʽΪ____������Fװ�����ռ�������������________��ͨ��(����a������b��)��
(2)��ij�����ռ�ʱֻ����Dװ���ռ����ɴ��Ƴ���������е�������_____________________��
(3)���ø��������ȡ����ʱ�����õķ���װ����_____________������Dװ���ռ�������֤���������ռ����ķ�����______________________________________��
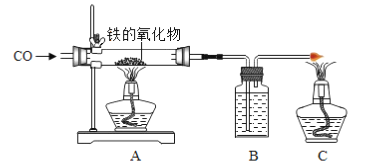
(4)ʵ������ȡ��������ʱ�����ü����Ȼ�粒������ʯ�ҹ��巴Ӧ��ȡ����֪������������ˮ���ܶ�С�ڿ�������ȡ�������õķ������ռ�װ����________________________��
(5)��30.9 g�����(KClO3)�Ͷ������̵Ĺ�������װ���Թ��У�������ȡ������ͬʱ�����Ȼ��ء�����Ӧ��ȫ���Թ���ȴ�����������Եõ�21.3 g�������ʡ������ԭ��������������ص�����Ϊ_________________��
���𰸡� BC 2H2O2 ![]() 2H2O + O2�� a ������ˮ���ܶȴ��ڿ��� A ��һ�������ǵ�ľ�����뼯��ƿ�ڴ�����ľ����ȼ��֤������ AE��AF 24.5
2H2O + O2�� a ������ˮ���ܶȴ��ڿ��� A ��һ�������ǵ�ľ�����뼯��ƿ�ڴ�����ľ����ȼ��֤������ AE��AF 24.5
��������(1)ʵ���Ҳ��÷ֽ����������Һ��ȡ����ʱ��Ҫ���Ʊ����ռ�װ��ΪBC�������Һ�巴Ӧ���������ȡ���壬������������ˮ����������ˮ�����÷�Ӧ�û�ѧ����ʽΪ��2H2O2 ![]() 2H2O + O2��������Fװ�����ռ������������ܶȱȿ�����������a��ͨ�롣(2)��ij�����ռ�ʱֻ����Dװ���ռ����ɴ��Ƴ���������е������ǡâ�������ˮ���ܶȴ��ڿ�����(3)���ø��������ȡ����ʱ�����õķ���װ����A�����������ȡ���壬����Dװ���ռ�������֤���������ռ����ķ����ǽ�һ�������ǵ�ľ�����뼯��ƿ�ڴ�����ľ����ȼ��֤��������(4)��ȡ�������õķ������ռ�װ����AE��AF��
2H2O + O2��������Fװ�����ռ������������ܶȱȿ�����������a��ͨ�롣(2)��ij�����ռ�ʱֻ����Dװ���ռ����ɴ��Ƴ���������е������ǡâ�������ˮ���ܶȴ��ڿ�����(3)���ø��������ȡ����ʱ�����õķ���װ����A�����������ȡ���壬����Dװ���ռ�������֤���������ռ����ķ����ǽ�һ�������ǵ�ľ�����뼯��ƿ�ڴ�����ľ����ȼ��֤��������(4)��ȡ�������õķ������ռ�װ����AE��AF��
���������ȡ���壬���弫������ˮ���ܶ�С�ڿ�����
(5)������ԭ��������������ص�����Ϊx
�������غ㶨��֪��������������Ϊ��30.9 g��21.3 g��9.6g��
2KClO3 ![]() 2KCl��3O2��
2KCl��3O2��
245 96
X 9.6g
![]() ��
��![]() ,x��24.5g��
,x��24.5g��
���ԭ��������������ص�����Ϊ24.5g��
�㾦�ø��ݷ�Ӧ��״̬�ͷ�Ӧ����ѡ����ȡ����װ�ã������������������ܽ��Ժ��ܶ�ѡ���ռ�������