题目内容
某校化学兴趣小组的同学准备对某生铁样品中铁的含量进行探究.请你按要求帮助他们完成下列探究报告.
[提出问题]生铁是纯铁吗?若不是纯铁则该生铁样品中铁单质的质量分数是多少?
[查阅资料](1)生铁中除铁外,还含有碳、硅、锰等元素.
(2)碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰等存在形式较为复杂.
(3)含有硅、锰等元素的物质通常都不与稀硫酸发生化学反应.
[制定方案]使生铁样品与过量的稀硫酸反应,称量反应前后物质的质量差.
[实验过程]
(1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(2)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
[数据处理]通过对以上数据的分析和计算,该生铁样品中铁单质的质量分数为 ______%.
[交流讨论]
(1)实验称量时称量物应放在托盘天平的 ______盘(选填“左”或“右”).
(2)实验过程中稀硫酸要过量的原因是 ______.
(3)反应过程中可看到有气泡冒出,溶液由无色变为浅绿色,由此得知反应一定生成了氢气和 ______(写名称).
(4)经质检部门精确测定,该样品中铁元素的总质量分数为95.2%.对此有同学产生了疑问,请你帮他分析:______.
[实验结论]经过以上探究,同学们知道了生铁不是纯铁,实际上它属于铁的重要 ______.
解:[数据处理]反应前后烧杯和剩余物质的总质量差即生成氢气的质量=102.4g+247.3g-348.7g=1g;
设参加反应单质铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 1g
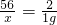 x=28g
x=28g
生铁样品中铁单质的质量分数=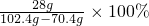 =87.5%
=87.5%
故答案为:87.5;
[交流讨论](1)使用天平称量物品的质量时,要遵循左物右码的使用原则,因此称量物应放在天平的左盘;
故答案为:左;
(2)生铁样品中铁单质的质量分数需要使单质与稀硫酸完全反应,为确保铁完全反应可通过加入过量的稀硫酸进行控制;
故答案为:确保生铁样品中铁单质与稀硫酸完全反应;
(3)铁与稀硫酸发生置换反应,生成硫酸亚铁和氢气,硫酸亚铁溶液呈浅绿色;
故答案为:硫酸亚铁;
(4)根据资料:碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);生铁样品中铁元素质量为单质铁的质量与Fe3C中铁元素质量之和;所以,该样品中铁元素的总质量分数为95.2%大于样品中铁单质的质量分数87.5%;
故答案为:生铁中的铁元素除了以单质形式存在还以Fe3C形式存在,所以铁单质的质量分数会小于铁元素的总质量分数;
[实验结论]生铁为含碳2%~4.3%的铁合金,而非纯次的单质铁;
故答案为:合金.
分析:[数据处理]生铁样品中单质铁与稀硫酸反应生成氢气,而其它成分不能与稀硫酸发生反应,因此,反应前后烧杯和剩余物质的总质量的差即为反应产生氢气的质量;利用氢气的质量,根据反应的化学方程式,可计算参加反应铁的质量及生铁样品中铁单质铁的质量分数;
[交流讨论](1)称量时,根据“左物右码”的原则称量物应放在天平的左盘;
(2)只有生铁中单质铁完全反应时,由产生氢气的质量计算所得铁的质量才是正确的结果,因此,实验中为确保单质铁完全反应,需要加入过量的稀硫酸;
(3)含Fe2+离子的溶液为浅绿色溶液,由生铁放入硫酸后观察到溶液由无色变为浅绿色,可判断溶液中含有硫酸亚铁;
(4)样品中铁元素的总质量包括单质铁的质量和化合物Fe3C中铁元素的质量;而生铁样品中铁单质的质量则不包括生铁中化合物Fe3C中的铁元素;
[实验结论]生铁和钢都是铁的合金,生铁为含碳2%~4.3%的铁合金.
点评:由于生铁中铁元素以游离铁和化合铁两种形态存在,因而出现了生铁中铁单质的质量分数会小于铁元素的总质量分数.
设参加反应单质铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 1g
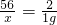 x=28g
x=28g生铁样品中铁单质的质量分数=
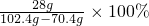 =87.5%
=87.5%故答案为:87.5;
[交流讨论](1)使用天平称量物品的质量时,要遵循左物右码的使用原则,因此称量物应放在天平的左盘;
故答案为:左;
(2)生铁样品中铁单质的质量分数需要使单质与稀硫酸完全反应,为确保铁完全反应可通过加入过量的稀硫酸进行控制;
故答案为:确保生铁样品中铁单质与稀硫酸完全反应;
(3)铁与稀硫酸发生置换反应,生成硫酸亚铁和氢气,硫酸亚铁溶液呈浅绿色;
故答案为:硫酸亚铁;
(4)根据资料:碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);生铁样品中铁元素质量为单质铁的质量与Fe3C中铁元素质量之和;所以,该样品中铁元素的总质量分数为95.2%大于样品中铁单质的质量分数87.5%;
故答案为:生铁中的铁元素除了以单质形式存在还以Fe3C形式存在,所以铁单质的质量分数会小于铁元素的总质量分数;
[实验结论]生铁为含碳2%~4.3%的铁合金,而非纯次的单质铁;
故答案为:合金.
分析:[数据处理]生铁样品中单质铁与稀硫酸反应生成氢气,而其它成分不能与稀硫酸发生反应,因此,反应前后烧杯和剩余物质的总质量的差即为反应产生氢气的质量;利用氢气的质量,根据反应的化学方程式,可计算参加反应铁的质量及生铁样品中铁单质铁的质量分数;
[交流讨论](1)称量时,根据“左物右码”的原则称量物应放在天平的左盘;
(2)只有生铁中单质铁完全反应时,由产生氢气的质量计算所得铁的质量才是正确的结果,因此,实验中为确保单质铁完全反应,需要加入过量的稀硫酸;
(3)含Fe2+离子的溶液为浅绿色溶液,由生铁放入硫酸后观察到溶液由无色变为浅绿色,可判断溶液中含有硫酸亚铁;
(4)样品中铁元素的总质量包括单质铁的质量和化合物Fe3C中铁元素的质量;而生铁样品中铁单质的质量则不包括生铁中化合物Fe3C中的铁元素;
[实验结论]生铁和钢都是铁的合金,生铁为含碳2%~4.3%的铁合金.
点评:由于生铁中铁元素以游离铁和化合铁两种形态存在,因而出现了生铁中铁单质的质量分数会小于铁元素的总质量分数.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
某校化学兴趣小组的同学经查阅资料知道:淀粉在适当温度和酸催化条件下可转变为葡萄糖.为探究淀粉在不同温度下转化为葡萄糖的程度,他们每人都进行了如下两步实验:
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
(2)在步骤2中A试管内所加Na0H溶液的作用是 .
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
| 现 象 | 结 论 | |
| 第一种 情 况 | A试管中: B试管中: | 淀粉没有转化为葡萄糖 |
| 第二种 情 况 | A试管中: B试管中: | |
| 第三种 情 况 | A试管中: B试管中: | 淀粉全部转化为葡萄糖 |
某校化学兴趣小组的同学经查阅资料知道:淀粉在适当温度和酸催化条件下可转变为葡萄糖.为探究淀粉在不同温度下转化为葡萄糖的程度,他们每人都进行了如下两步实验:
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
(2)在步骤2中A试管内所加Na0H溶液的作用是 .
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
| 现 象 | 结 论 | |
| 第一种 情 况 | A试管中: B试管中: | 淀粉没有转化为葡萄糖 |
| 第二种 情 况 | A试管中: B试管中: | |
| 第三种 情 况 | A试管中: B试管中: | 淀粉全部转化为葡萄糖 |
