题目内容
【题目】某同学将一定质量的碳酸氢钠和稀硫酸混合,反应完全后(假设反应产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:
(实验用品)pH试纸、Zn片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(假设猜想)
猜想一:硫酸钠;
猜想二:硫酸钠、碳酸氢钠;
猜想三:硫酸钠、硫酸;
猜想四:硫酸钠、碳酸氢钠、硫酸。
经分析猜想四不正确,因为________________(用化学方程式表示)。
(实验探究)同学们取反应后的溶液用不同方案进行如下实验:
(1)取少量反应后的溶液于试管中,滴加稀硫酸,观察到___________,则猜想二错误;
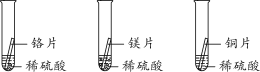
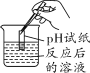
(2)如图所示进行实验,试纸变色,对照比色卡,pH______7(填“>”、“<”或“=”),猜想三正确。
(讨论)(1)小丽认为还可选择Zn片、氧化铜粉末进行实验,预测可观察到的现象分别为_____;黑色粉末逐渐溶解,溶液由无色变为________色。
(2)小明认为也可向反应后溶液中滴加氯化钡溶液,产生白色沉淀,也能得出结论。
(评价反思)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究和讨论中存在两处明显错误。分别是:①_______________;②_____________。
【答案】2NaHCO3+H2SO4= Na2SO4+2H2O+2CO2↑ 无气泡产生 < 有气泡产生,锌片不断溶解 蓝 实验(2)中pH试纸直接浸入溶液中 硫酸钠与氯化钡反应也会产生白色沉淀,不能证明反应后溶液中一定含有硫酸
【解析】
略

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目