题目内容
写出下列反应的化学方程式。
(1)工业炼铁的主要反应原理:______
(2)含小苏打的药物治疗胃酸过多症:_____
(3)用稀盐酸除去铝片表面的氧化膜:_______
(4)工业上用贝壳、石灰石、白垩等物质制取生石灰:_______
(5)天然气完全燃烧:_______
小明同学对本学期所学的某些科学知识归纳如下,其中完全正确的是( )
A.生活中的安全常识 使煤燃烧更旺:把煤做成蜂窝状 夜间发现天然气泄漏:立即开灯寻找泄漏 酒精灯不慎着火:可以用湿布灭火 | B.性质和用途关系 氦气:密度小,可用作探空气球 氧气:助燃性,可用作火箭的 燃料 红磷:燃烧产生白烟,可用于制作烟幕弹 |
C.化学常见的“三” 地壳中含量最高的三种元素:氧、硅、铝 可以直接加热的三种仪器:试管、坩埚、蒸发皿 构成物质的三种基本粒子:分子、原子、离子 | D.事实与解释 量筒量取一定体积液体时,所得液体偏少:仰视读数 氮气被压缩成液氮:分子之间有间隔 水和过氧化氢化学性质不同:分子构成 不同 |
A. A B. B C. C D. D
工业上常采用“双碱法”除去烟气中的 ,工业流程示意图如下.
,工业流程示意图如下.

(1)吸收塔中,用NaOH溶液吸收 ,化学反应方程式是___.NaOH溶液喷成雾状能充分吸收SO2的原因是_____
,化学反应方程式是___.NaOH溶液喷成雾状能充分吸收SO2的原因是_____
(2)氧化室中,化学反应方程式是_______。
(3)已知部分原料的价格如表所示.
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.90 |
上述工业流程中,处理相同量的 ,双碱法所需的原料成本比用NaOH直接吸收更低,原因是___
,双碱法所需的原料成本比用NaOH直接吸收更低,原因是___
(4)某中学化学兴趣小组为测定工厂周围的空气中的二氧化硫含量是否符合国家标准,将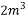 周围空气通入一定含量碘(
周围空气通入一定含量碘(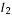 )2.54mg的碘水中,经测定I2与二氧化硫恰好完全反应,该反应的化学方程式是
)2.54mg的碘水中,经测定I2与二氧化硫恰好完全反应,该反应的化学方程式是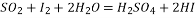 。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别______。
。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别______。
[资料信息:我国空气质量标准对空气中二氧化硫的浓度级别规定如下表所示(空气中二氧化硫的浓度用单位体积的空气中所含二氧化硫的质量表示)]。
浓度级别 | 标准(mg·m-3) |
一级 | 浓度≤0.15 |
二级 | 0.15<浓度≤0.50 |
三级 | 0.50<浓度≤0.70 |
兴趣小组的同学对做完氢氧化钠与稀硫酸反应后溶液中溶质的成分进行了探究,请和他们一起完成实验探究。
(提出问题)溶液中溶质的成分是什么?
(做出猜想)猜想一:Na2SO4;猜想二:Na2SO4和_____;猜想三:Na2SO4和NaOH.猜想四:Na2SO4、NaOH和H2SO4。
(查阅资料)①Na2SO4溶液显中性;②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)、水和氢气。
实验操作 | 实验现象 | 实验结论 | |
甲同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出 | 猜想二成立 |
乙同学实验 | 取中和反应后的溶液少许于另一试管中,项试管中滴加几滴无色酚酞试液 | 溶液变_____色 | 猜想三成立 |
(交流反思)①同学们一致认为猜想四不成立,理由是_____(用化学方程式回答)。
②丙同学对甲同学实验的准确性提出了疑义,其理由是_____。丙同学认为要想验证猜想二是否成立,可以将药品换为_____或_____(填两类不同物质名称),若通过观察没有气泡产生,则可以证明猜想二_____。
③该组同学经过充分讨论,一致认为猜想三成立,则甲同学的实验是铝片和_____发生的反应。


 )、赤铜矿(
)、赤铜矿( )和木炭粉混合加热到约800℃左右,得到一种外观似金子的锌和铜的合金。该过程发生反应:
)和木炭粉混合加热到约800℃左右,得到一种外观似金子的锌和铜的合金。该过程发生反应: ;再通过木炭粉还原氧化锌,赤铜矿获得金属锌和铜。若要得到含铜80%的锌和铜的合金80t,需要含
;再通过木炭粉还原氧化锌,赤铜矿获得金属锌和铜。若要得到含铜80%的锌和铜的合金80t,需要含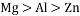
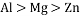

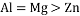
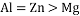
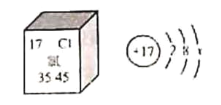
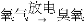 ,下列说法正确的是( )
,下列说法正确的是( )