题目内容
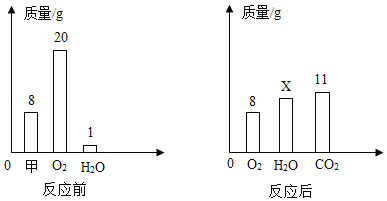
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示。下列说法正确的是( )
A.X的值是9
B.该反应属于置换反应
C.甲由碳、氢、氧三种元素组成
D.甲中碳、氢元素的原子个数比为1:3
【答案】C
【解析】
由于四种物质中甲和氧气质量减小,所以是反应物,且反应物的总质量是8g+(20g﹣8g)=20g,而水和二氧化碳的质量的质量增加,依据质量守恒定律参加化学反应的各物质质量总和等于反应后生成的各物质质量总和,所以X的值是(8+20+1﹣8﹣11)g=10g,即生成水的质量为10g﹣1g=9g;此反应的表达式可表示为甲+O2→CO2+H2O。
A、由以上分析可知,X的值是10,故错误;
B、该反应的生成物是两种化合物,不属于置换反应,故错误;
C、根据质量守恒定律,由反应表达式可以看出甲中一定含有碳氢两种元素,是否含有氧元素则要通过生成物中的氧元素与反应的氧气质量进行比较,生成的水中氧元素的质量为:9g×![]() ×100%=8g,二氧化碳中氧元素的质量:11g×
×100%=8g,二氧化碳中氧元素的质量:11g×![]() ×100%=8g,两者的质量和为16g,而参加反应的氧气的质量20g﹣8g=12g,所以可判断W中含有氧元素,故正确;
×100%=8g,两者的质量和为16g,而参加反应的氧气的质量20g﹣8g=12g,所以可判断W中含有氧元素,故正确;
D、甲物质中,碳、氢元素的原子个数比为: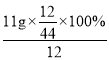 :
: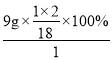 =1:4,故错误。
=1:4,故错误。
故选C。

练习册系列答案
相关题目
【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
选项 | A | B | C | D |
实 验 装 置 |
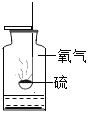
硫在氧气中燃烧 |
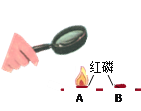
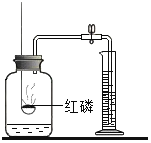
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:用水将集气瓶内的空气排净后,便于观察O2何时收集满 |
A.AB.BC.CD.D