题目内容
海洋是人类的母亲,是人类千万年来取之不尽、用之不竭的巨大资源宝库.我国有较长的海岸线,海洋资源十分丰富.以下是我国对海水资源的部分利用.
(1)海水中含量最高的盐是______(写化学式),海水经______结晶可获得粗盐.
(2)粗盐中含有泥沙、硫酸镁、氯化钙等杂质.将粗盐溶于水,然后再进行如下操作即可得到较纯的氯化钠:①过滤;②加过量的NaOH溶液;③加适量的盐酸;④加过量的Na2CO3溶液;⑤加过量的BaCl2溶液.正确的操作顺序是______.
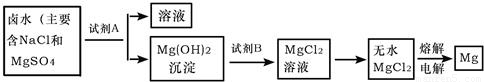
(3)从晒盐后的卤水中提取重要金属镁.提取镁的步骤如下:
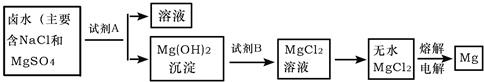
提取镁的过程中,试剂A最好选用______(写化学式),试剂B选用______(写名称).电解无水氯化镁的过程中______能转化为______能,写出电解氯化镁的化学反应方程式:______.
(4)向饱和的氯化钠溶液中依次通入氨气、二氧化碳,析出碳酸氢钠晶体,加热碳酸氢钠晶体可制得纯碱.写出上述反应的化学方程式:
①______;
②______.
(5)制得的纯碱在生产、生活中具有广泛用途:
①生活中纯碱常用做洗涤剂,洗涤餐具,原因是纯碱的溶液显______性.
②工业上用纯碱和石灰石为原料制烧碱,写出制取过程中所发生反应的化学方程式:______.
③工业上通常用纯碱、石英砂、石灰石混合高温煅烧制玻璃,写出制取过程中所发生反应的化学方程式:
______.
解:(1)海水中含量最高的盐是氯化钠.故填:NaCl.
海水经蒸发结晶可获得粗盐.故填:蒸发.
(2)要除去粗盐中含有的杂质,可以加过量的氯化钡溶液除去硫酸镁,加过量的NaOH溶液除去镁离子,加过量的Na2CO3溶液除去氯化钙,通过过滤把不溶于水的物质除去,加适量的盐酸除去过量的氢氧化钠和碳酸钠.故填:⑤②④①③.
(3)提取镁的过程中,试剂A最好选用氢氧化钙,因为氢氧化钙比较经济.故填:Ca(OH)2.
试剂B选用稀盐酸.故填:稀盐酸.
电解氯化镁的过程中电能转化成化学能.故填:电;化学.
电解氯化镁的化学反应方程式:MgCl2 Mg+Cl2↑.
Mg+Cl2↑.
(4)向饱和的氯化钠溶液中依次通入氨气、二氧化碳,析出碳酸氢钠晶体,加热碳酸氢钠晶体可制得纯碱.上述反应的化学方程式分别为:
①NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl;
②2NaHCO3 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.
(5)①生活中纯碱常用做洗涤剂,洗涤餐具,原因是纯碱的溶液显碱性.故填:碱.
②工业上用纯碱和石灰石为原料制烧碱,制取过程中所发生反应的化学方程式分别为:CaCO3 CaO+CO2↑、CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
CaO+CO2↑、CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
③工业上通常用纯碱、石英砂、石灰石混合高温煅烧制玻璃,制取过程中所发生反应的化学方程式:CaCO3+SiO2 CaSiO3+CO2↑、Na2CO3+SiO2
CaSiO3+CO2↑、Na2CO3+SiO2 Na2SiO3+CO2↑.
Na2SiO3+CO2↑.
分析:电解氯化镁的过程中电能转化成化学能;根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式.
点评:解答本题要掌握化学方程式的书写方法和能量之间的转化关系,只有这样才能对相关方面的问题做出正确的判断.
海水经蒸发结晶可获得粗盐.故填:蒸发.
(2)要除去粗盐中含有的杂质,可以加过量的氯化钡溶液除去硫酸镁,加过量的NaOH溶液除去镁离子,加过量的Na2CO3溶液除去氯化钙,通过过滤把不溶于水的物质除去,加适量的盐酸除去过量的氢氧化钠和碳酸钠.故填:⑤②④①③.
(3)提取镁的过程中,试剂A最好选用氢氧化钙,因为氢氧化钙比较经济.故填:Ca(OH)2.
试剂B选用稀盐酸.故填:稀盐酸.
电解氯化镁的过程中电能转化成化学能.故填:电;化学.
电解氯化镁的化学反应方程式:MgCl2
 Mg+Cl2↑.
Mg+Cl2↑.(4)向饱和的氯化钠溶液中依次通入氨气、二氧化碳,析出碳酸氢钠晶体,加热碳酸氢钠晶体可制得纯碱.上述反应的化学方程式分别为:
①NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl;
②2NaHCO3
 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.(5)①生活中纯碱常用做洗涤剂,洗涤餐具,原因是纯碱的溶液显碱性.故填:碱.
②工业上用纯碱和石灰石为原料制烧碱,制取过程中所发生反应的化学方程式分别为:CaCO3
 CaO+CO2↑、CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
CaO+CO2↑、CaO+H2O═Ca(OH)2、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.③工业上通常用纯碱、石英砂、石灰石混合高温煅烧制玻璃,制取过程中所发生反应的化学方程式:CaCO3+SiO2
 CaSiO3+CO2↑、Na2CO3+SiO2
CaSiO3+CO2↑、Na2CO3+SiO2 Na2SiO3+CO2↑.
Na2SiO3+CO2↑.分析:电解氯化镁的过程中电能转化成化学能;根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式.
点评:解答本题要掌握化学方程式的书写方法和能量之间的转化关系,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
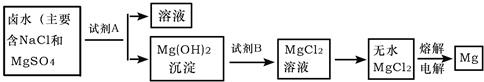
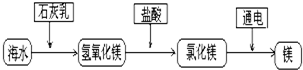 海洋是人类的母亲.浩瀚的海洋不仅繁衍着无数水生生物,还蕴藏着丰富的化学资源,如氯化钠、氯化钙、氯化镁、溴化镁等大量的无机盐.
海洋是人类的母亲.浩瀚的海洋不仅繁衍着无数水生生物,还蕴藏着丰富的化学资源,如氯化钠、氯化钙、氯化镁、溴化镁等大量的无机盐.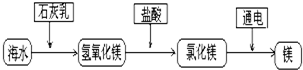 海洋是人类的母亲.浩瀚的海洋不仅繁衍着无数水生生物,还蕴藏着丰富的化学资源,如氯化钠、氯化钙、氯化镁、溴化镁等大量的无机盐.
海洋是人类的母亲.浩瀚的海洋不仅繁衍着无数水生生物,还蕴藏着丰富的化学资源,如氯化钠、氯化钙、氯化镁、溴化镁等大量的无机盐.