题目内容
 如图是三种固体物质的溶解度曲线.
如图是三种固体物质的溶解度曲线.(1)物质c的溶解度随温度的升高而
(2)将t1℃时a、b、c三种物质的饱和溶液升温至t2℃(溶剂量不变),溶液中溶质质量分数不变的是
(3)将t2℃时相同质量a、b、c三种物质的饱和溶液降温至t1℃,析出晶体最多的是
(4)若b为氯化钠,那么从它的饱和溶液中获得较多的氯化钠晶体,应采取
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)由图可知,物质c的溶解度随温度变化的趋势;
(2)据a、b、c三种物质的溶解度随温度变化情况,及溶质的质量分数计算分析解答;
(3)由溶解度曲线图,对比abc三物质溶解度受温度影响大小,判断晶体析出情况;
(4)结合物质的溶解度随温度变化情况分析解答.
(2)据a、b、c三种物质的溶解度随温度变化情况,及溶质的质量分数计算分析解答;
(3)由溶解度曲线图,对比abc三物质溶解度受温度影响大小,判断晶体析出情况;
(4)结合物质的溶解度随温度变化情况分析解答.
解答:解:(1)物质c的溶解度随温度的升高而减小;
(2)由图可知:ab的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,故将t1℃时a、b、c三种物质的饱和溶液升温至t2℃(溶剂量不变),ab变为不饱和溶液,溶质的质量不变,溶剂的质量不变,则溶液中溶质质量分数不变,c溶解度减小,要析出晶体,溶质的质量分数减小;
(3)由溶解度曲线图,对比abc三物质溶解度受温度影响大小,可以知道t2℃时三种物质的溶解度a>b>c,从t2℃降温到t1℃,A的溶解度变化较大,所以A析出的较多.
(4)b的溶解度受温度影响不大,那么从它的饱和溶液中获得较多的氯化钠晶体,可采用蒸发结晶的方法;
故答案为:(1)减小;
(2)ab;
(3)a;
(4)蒸发结晶
(2)由图可知:ab的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,故将t1℃时a、b、c三种物质的饱和溶液升温至t2℃(溶剂量不变),ab变为不饱和溶液,溶质的质量不变,溶剂的质量不变,则溶液中溶质质量分数不变,c溶解度减小,要析出晶体,溶质的质量分数减小;
(3)由溶解度曲线图,对比abc三物质溶解度受温度影响大小,可以知道t2℃时三种物质的溶解度a>b>c,从t2℃降温到t1℃,A的溶解度变化较大,所以A析出的较多.
(4)b的溶解度受温度影响不大,那么从它的饱和溶液中获得较多的氯化钠晶体,可采用蒸发结晶的方法;
故答案为:(1)减小;
(2)ab;
(3)a;
(4)蒸发结晶
点评:本题难度不是很大,主要考查了根据固体的溶解度曲线解决相关的问题,培养学生的分析能力和解题能力.

练习册系列答案
相关题目
下列各组都是生活中常见的物质,其中属于同一类物质的一组是( )
| A、红磷 医用酒精 烧碱 |
| B、甲烷 加碘盐 石灰水 |
| C、食醋 液氧 酱油 |
| D、海水 天然气 石油 |
下列变化不属于化学变化的是( )
| A、用活性炭净化水 |
| B、铁矿石炼铁 |
| C、植物的光合作用 |
| D、煤气燃烧 |

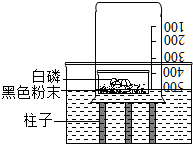 在按书本装置测定空气中氧气含量的实验时,当装置内的氧气低于一定含量时,红磷就不再与氧气反应,从而导致测量结果偏小.有老师对该实验进行了改进,装置如图所示,在一容器中倒入刚拆封的“暖宝宝”黑色粉末,再在上面放足量的白磷,迅速扣上烧杯,随后白磷自燃,利用这一装置可更准确地测定空气中氧气的体积分数.
在按书本装置测定空气中氧气含量的实验时,当装置内的氧气低于一定含量时,红磷就不再与氧气反应,从而导致测量结果偏小.有老师对该实验进行了改进,装置如图所示,在一容器中倒入刚拆封的“暖宝宝”黑色粉末,再在上面放足量的白磷,迅速扣上烧杯,随后白磷自燃,利用这一装置可更准确地测定空气中氧气的体积分数.
 某兴趣小组同学按照下图实验装置进行实验,请回答相关问题:
某兴趣小组同学按照下图实验装置进行实验,请回答相关问题: