题目内容
将KClO3和MnO2的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,求
(1)产生O2的质量;
(2)原混合物中MnO2的质量.
解:设生成氧气的质量为x.
2KClO3 2KCl+3O2↑
2KCl+3O2↑
149 96
100g×7.45% x
(1)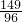 =
= ,x=4.8g
,x=4.8g
(2)MnO2的质量为:15.5g-(100g×7.45%+4.8g)=3.25g
答:(1)产生4.8g氧气;(2)二氧化锰的质量为3.25g.
分析:根据溶质质量分数的相关计算可得氯化钾的质量,由氯化钾的质量根据化学方程式计算出产生氧气的质量和发生反应的氯酸钾的质量,进而计算出二氧化锰的质量.
点评:本题主要考查溶质质量分数的相关计算、有关化学方程式的计算和质量守恒定律,难度稍大.
2KClO3
 2KCl+3O2↑
2KCl+3O2↑149 96
100g×7.45% x
(1)
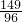 =
= ,x=4.8g
,x=4.8g(2)MnO2的质量为:15.5g-(100g×7.45%+4.8g)=3.25g
答:(1)产生4.8g氧气;(2)二氧化锰的质量为3.25g.
分析:根据溶质质量分数的相关计算可得氯化钾的质量,由氯化钾的质量根据化学方程式计算出产生氧气的质量和发生反应的氯酸钾的质量,进而计算出二氧化锰的质量.
点评:本题主要考查溶质质量分数的相关计算、有关化学方程式的计算和质量守恒定律,难度稍大.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
现将KClO3和MnO2的固体混合物30.5g,放入制氧气的装置中加热至不再产生气体为止,收集到一定质量的O2.某同学欲求得所制O2的质量,他将加热后剩余物质冷却到一定温度后,通过多次加水测定剩余固体质量的办法来求出.加水的质量与剩余固体的质量见下表:
试求:(1)表中X的值为 .(2)所制得氧气的质量.
| 加水次第 | 1 | 2 | 3 | 4 |
| 加水的质量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 14.5 | 8.1 | X | 6 |
现将KClO3和MnO2的固体混合物30.5g,放入制氧气的装置中加热至不再产生气体为止,收集到一定质量的O2.某同学欲求得所制O2的质量,他将加热后剩余物质冷却到一定温度后,通过多次加水测定剩余固体质量的办法来求出.加水的质量与剩余固体的质量见下表:
| 加水次第 | 1 | 2 | 3 | 4 |
| 加水的质量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 14.5 | 8.1 | X | 6 |