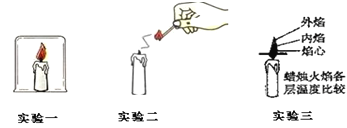
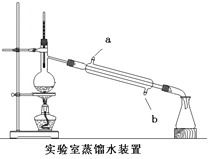
题目内容
【题目】为了探究二氧化锰是否对氯酸钾的分解起了催化作用,经查阅资料得知;氯酸钾的熔点为356℃,加热到400℃可观察到缓慢放出气泡。实验仪器如下:
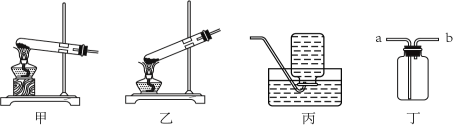
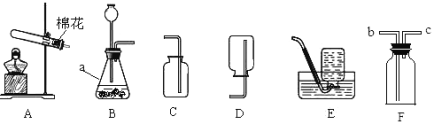
(1)①验设计如下,请你补充完成实验报告。
实验步骤 | 加热时间(分钟) | 实验现象 |
1.将二氧化锰单独放入试管中加热,将带火星的木条放在试管口 | 10 | 木条无变化 |
2.将氯酸钾单独放入试管中加热,将带火星的木条放在试管口 | 5 | 木条复燃 |
3.将____________________________,将带火星的木条放在试管口 | 1 | 木条复燃 |
②该实验方法称为______________________,第二步试验中,某同学选用装置乙加热,你认为是否正确?理由是__________________________________________。
③写出第三步实验中发生的化学反应方程式___________________________。
(2)“丙”中除导管外,另两个玻璃仪器的名称为____________、_____________;若用装置“丁”收集氧气,则导出气体的导管口是_____________(填写编号“a”或“b”)。
(3)实验室制取氧气还可用双氧水作为原料,比较用氯酸钾为原料的制取方法,用双氧水作原料的方案突出的优点是___________________(填写选项编号)
A.不需要加热,操作简单
B.通过分液漏斗加液体,有利于连续操作
C.节约药品
D.可以使用启普发生器,使制取更方便
【答案】(1)①二氧化锰和氯酸钾混合均匀后放入试管中加热;
②对照(或对比、控制变量法);合理,因为氯酸钾的熔点比其分解的温度低,防止倒流(或氯酸钾分解时已经是液态,合理即可)
③2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(2)集气瓶、水槽;b;(3)AB
【解析】
试题分析:(1)①根据题中表格中的内容,结合催化剂的特点就可以补充完全实验步骤,第3步应为将二氧化锰和氯酸钾混合均匀后放入试管中加热,将带火星的木条放在试管口;②题中做的不同实验都是为了与其他试验作比较,该实验方法称为对照;第二步实验“将氯酸钾单独放入试管中加热,将带火星的木条放在试管口”,由于氯酸钾分解的温度小于其熔化的温度,这就要求试管口必须稍向上倾斜,防止液态氯酸钾流出;
(2)“丙”为排水法收集氧气,用到的玻璃仪器有导气管、水槽和集气瓶;由于氧气的密度比空气大,用排空气法收集氧气必须采用口向上排空气法,若用装置“丁”收集氧气,则导出气体的导管口是b;
(3)A.用过氧化氢制取氧气不需要加热,操作简单,A选项说法正确;
B.用过氧化氢制取氧气时可通过分液漏斗加液体,有利于连续操作,B选项说法正确;
C.哪种方法制取氧气都需要消耗药品,C选项不符合题意;
D.该反应中催化剂二氧化锰是粉末药品,不能使用启普发生器,故D选项不符合题意。