题目内容
某学生书写的下列化学方程式,其中正确的是
- A.Cu+2HCl=CuCl2+H2↑
- B.2Fe+6HCl=2FeCl3+3H2↑
- C.Zn+2HNO3(稀)=Zn(NO3)2+H2↑
- D.Mg+H2SO4=MgSO4+H2↑
D
分析:A、根据金属活动性顺序进行分析;
B、根据铁在置换反应中常显示+2价进行分析;
C、根据活泼金属与硝酸反应不会生成氢气进行分析;
D、根据方程式的书写规则进行分析.
解答:A、铜在金属活动性顺序中排在氢之后,不会置换出酸中的氢,故A错误;
B、铁遇酸发生置换反应时,常显示+2价,正确的方程式为:Fe+2HCl=FeCl2+H2↑,故B错误;
C、锌和硝酸反应生成水而不会生成氢气,故C错误;
D、该方程式应用原理正确,化学式符合客观规律,满足质量守恒定律,故D正确;
故选D.
点评:在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断.
分析:A、根据金属活动性顺序进行分析;
B、根据铁在置换反应中常显示+2价进行分析;
C、根据活泼金属与硝酸反应不会生成氢气进行分析;
D、根据方程式的书写规则进行分析.
解答:A、铜在金属活动性顺序中排在氢之后,不会置换出酸中的氢,故A错误;
B、铁遇酸发生置换反应时,常显示+2价,正确的方程式为:Fe+2HCl=FeCl2+H2↑,故B错误;
C、锌和硝酸反应生成水而不会生成氢气,故C错误;
D、该方程式应用原理正确,化学式符合客观规律,满足质量守恒定律,故D正确;
故选D.
点评:在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
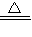 Hg+O2↑
Hg+O2↑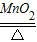 KCl+3O2↑
KCl+3O2↑  CO2↑
CO2↑  MgO
MgO  2P2O5
2P2O5 Hg+O2↑
Hg+O2↑ KCl+3O2↑
KCl+3O2↑  CO2↑
CO2↑  MgO
MgO  2P2O5
2P2O5