题目内容
【题目】小新用20 g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下。请计算:
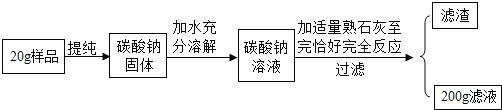
(1)20 g样品中碳酸钠的质量为多少g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
【答案】(1)10.6
(2)设反应生成氢氧化钠的质量为x。
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
106 80
10.6 g x
![]() =
=![]() x=8 g
x=8 g
反应后滤液中氢氧化钠的质量分数为![]() ×100%=4%
×100%=4%
答:反应后所得滤液中氢氧化钠的质量分数为4%。
【解析】解:(1)20 g样品中碳酸钠的质量为20g×53%=10.6g
(2)设反应生成氢氧化钠的质量为x。
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
106 80
10.6 g x
![]()
x=8 g
反应后滤液中氢氧化钠的质量分数为![]() ×100%=4%
×100%=4%
答:反应后所得滤液中氢氧化钠的质量分数为4%。

练习册系列答案
相关题目