题目内容
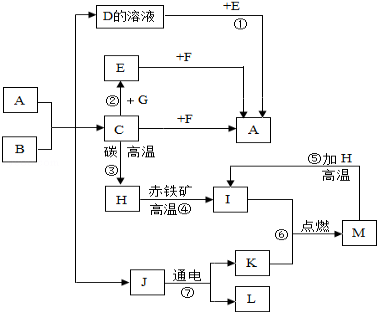
【题目】A~M均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,F是澄清石灰水主要成分,E是钠盐,它们之间有如图所示的相互转换关系(图中部分生成物已略去).请回答下列问题:
(1)E的俗称为 ,请画出K所含元素的原子结构示意图 .
(2)通电电解J时,通常加入少量烧碱或硫酸的目的是 ,电解一段时间后在相同条件下,生成气体L和气体K的体积之比约为 .
(3)请写出I在K中燃烧时的现象 ;⑥的基本反应类型为 .
(4)请写出⑤的化学方程式 .
【答案】(1)纯碱或苏打; ;
;
(2)增加水的导电性,2:1;
(3)火星四射、有黑色固体生成、并放出热量;化合反应;
(4)4CO+Fe3O4![]() 3Fe+4CO2.
3Fe+4CO2.
【解析】
试题分析:(1)由于A是大理石主要成分,故A是碳酸钙,B是人体胃酸的一种主要成分,故B是盐酸,F是澄清石灰水主要成分,所以F是氢氧化钙,A和B反应能够生成水(J通电能分解)D的溶液氯化钙溶液,和气体二氧化碳C,二氧化碳能与石灰水反应生成沉淀碳酸钙A,氯化钙的溶液能够和碳酸盐的溶液反应生成碳酸钙,E是钠盐,所以E是碳酸钠,二氧化碳能够和碳在高温的体检下生成一氧化碳,一氧化碳可以与氧化铁反应生成铁,铁能在氧气中燃烧生成四氧化三铁,故可知H是一氧化碳,I是铁,M是四氧化三铁,K是氧气,L是氢气;
(1)由分析知E是碳酸钠,俗称纯碱或苏打;K所含元素的原子是氧原子,其原子结构示意图是 ;
;
(2)纯水不易导电,所以通电电解水时,通常加入少量烧碱或硫酸的目的是增加导电性,通电后生成的氢气和氧气的体积比是2:1;
(3)铁在氧气中燃烧的现象是:火星四射、有黑色固体生成、并放出热量,该反应的反应物是氧气和铁生成物是四氧化三铁,所以符合“多变一”的化合反应特点;
(4)反应⑤是一氧化碳和四氧化三铁的反应,方程式为:4CO+Fe3O4![]() 3Fe+4CO2.
3Fe+4CO2.