题目内容
【题目】配制50g一定溶质质量分数的氯化钠溶液,实验步骤如下:
(1)计算:氯化钠质量和水的体积(水的密度:1.0g/mL).
(2)称量:如图所示(右盘无砝码)称量的氯化钠质量为________g.
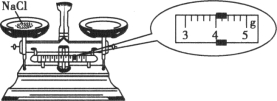
量取:选择________(填“30”“50”或“100”)mL的量筒准确量取________水.
(3)溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解,配得的氯化钠溶液中溶质的质量分数为________.
(4)装瓶、贴标签:请填写图所示标签.

【反思】
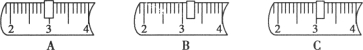
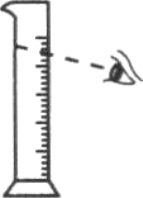
(5)上述实验过程中,用量筒量取水时,若按图方式进行读数,将导致所配溶液的溶质质量分数________(填“偏大”“不变”或“偏小”).
【答案】(2)4.0 50 46.0mL (3)8%
(4)
(5)偏小
【解析】(2)从托盘天平的读数可知称量的氯化钠质量为4.0g;由于所配溶液的质量为50g,所以需要水的质量为46.0g,应用50mL的量筒量取46.0mL水.(3)根据溶质质量分数的计算公式,可求所配溶液的溶质质量分数为![]() .(4)填写标签,上面是溶质的质量分数,下面是溶液的名称.(5)用量筒量取水时,若仰视读数,所取水会偏多,配得溶液的溶质质量分数会偏小.
.(4)填写标签,上面是溶质的质量分数,下面是溶液的名称.(5)用量筒量取水时,若仰视读数,所取水会偏多,配得溶液的溶质质量分数会偏小.

练习册系列答案
相关题目