题目内容
(2006?包头)现有铁片、铜片、硝酸汞溶液和稀盐酸四种物质,要通过实验来确定Fe、Cu、Hg的活动性顺序.有如下二种方案:
A.铁放入稀盐酸中,铜放入稀盐酸中,铁放入硝酸汞溶液中
B.铁放入稀盐酸中,铜放入稀盐酸中,铜放入硝酸汞溶液中
以上方案不合理的是
A.铁放入稀盐酸中,铜放入稀盐酸中,铁放入硝酸汞溶液中
B.铁放入稀盐酸中,铜放入稀盐酸中,铜放入硝酸汞溶液中
以上方案不合理的是
A
A
(填字母),理由是无法判断Cu和Hg的活动性强弱
无法判断Cu和Hg的活动性强弱
.分析:根据金属与酸、盐反应的规律,通过分析方案所能得到的结论,得出能否确定Fe、Cu、Hg三种金属的活动性顺序的方案.
解答:解:A、铁与盐酸反应放出氢气,说明了活动性铁>氢;铜与盐酸不能反应,说明了活动性铜<氢;铁与硝酸汞反应置换出汞,说明活动性铁>汞;方案没有确定铜与汞的活动性关系;故方案不合理;
铁与盐酸反应放出氢气,说明了活动性铁>氢;铜与盐酸不能反应,说明了活动性铜<氢;铜与硝酸汞反应置换出汞,说明活动性铜>汞;由此方案可得到的三种金属活动性铁>铜>汞;故方案合理;
故答案为:A、无法判断Cu和Hg的活动性强弱
铁与盐酸反应放出氢气,说明了活动性铁>氢;铜与盐酸不能反应,说明了活动性铜<氢;铜与硝酸汞反应置换出汞,说明活动性铜>汞;由此方案可得到的三种金属活动性铁>铜>汞;故方案合理;
故答案为:A、无法判断Cu和Hg的活动性强弱
点评:活动性强的金属能将活动性弱的金属从其盐溶液中置换出来,活动性顺序中位于氢之前的金属能与酸反应放出氢气.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
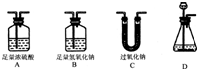 (2006?包头)过氧化钠(Na2O2)是一种淡黄色固体,它能与二氧化碳反应生成氧气.此外,过氧化钠还能与水反应生成氧气.反应的化学方程式分别为:2Na2O2+2CO2═2Na2CO3+
(2006?包头)过氧化钠(Na2O2)是一种淡黄色固体,它能与二氧化碳反应生成氧气.此外,过氧化钠还能与水反应生成氧气.反应的化学方程式分别为:2Na2O2+2CO2═2Na2CO3+