题目内容
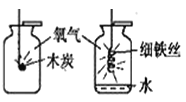
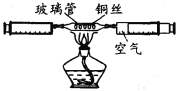
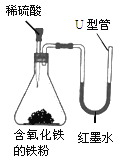
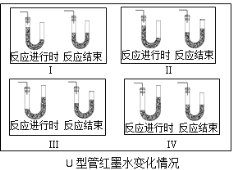
【题目】(7分)下图是实验探究氢气与氧气混合点燃发生爆炸的条件:
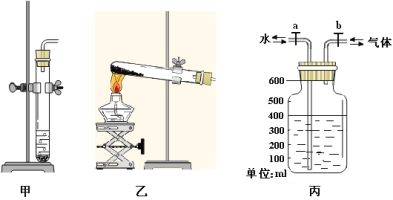
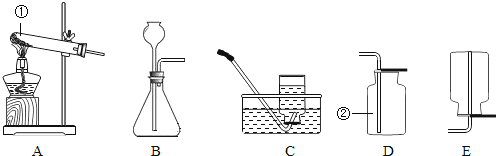
⑴乙装置中对试管加热的仪器名称是 ;在实验室中利用氯酸钾和二氧化锰制取氧气,反应的化学方程式是 ;利用锌粒和稀硫酸制取氢气,可以利用下列
(选填“甲”或“乙”)作为发生装置。
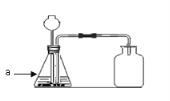
⑵利用丙装置可将氢气、氧气收集并混合起来。某次实验的操作过程如下:先将瓶子装满水,打开a、b,从右边导管通入氢气至水面降至400mL,水从左边导管流出(如图),然后继续从右边导管通入氧气至液面降到100mL,关闭b。此时瓶中收集到的混合气体中氢气与氧气的体积比为 。打开b,再从左边导管向瓶中加水,使混合气体全部排出,并用一次性保鲜袋收集,直接点燃保鲜袋内的混合气体。实验共四次,实验数据及现象记录如下表,请将表中漏填的数据及现象补填上。
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
氢气与氧气的体积比 | 1︰4 | 2︰3 | 2︰1 | 4︰1 |
氢气的体积百分数 | 20% | 40% | % | 80% |
点燃后现象 | 爆炸 |
| 爆炸 | 保鲜袋燃烧,没有爆炸 |
由此可见氢气与氧气混合发生爆炸,除要达到燃烧的三个条件外,还和氢气的体积分数有关。
【答案】 ⑴酒精灯 2KClO3![]() 2KCl+3O2↑ 甲
2KCl+3O2↑ 甲
⑵2︰3 66.7 爆炸
【解析】
试题分析:(1)用于加热的仪器是酒精灯;实验室中利用氯酸钾和二氧化锰制取氧气生成的是氯化钾和氧气:2KClO3![]() 2KCl+3O2↑;利用锌粒和稀硫酸制取氢气,属固液在常温下的反应,应选甲装置;
2KCl+3O2↑;利用锌粒和稀硫酸制取氢气,属固液在常温下的反应,应选甲装置;
(2)通入氢气至水面降至400mL,所以氢气体积为:600mL-400mL=200mL;继续从右边导管通入氧气至液面降到100mL,所以氧气体积为:400mL-100mL=300mL;混合气体中氢气与氧气的体积比为:200mL:300mL=2:3;氢气的体积分数是:2/3 ×100%=66.7%;根据第一次和第三次现象可知第二次现象是爆炸.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案