��Ŀ����
����Ŀ���ڹ�ҵ��ͨ���ô����ʯ��ʯΪԭ���Ʊ��ռ����Ҫ������ͼ��ʾ��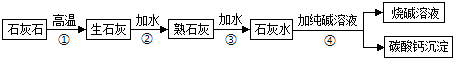
��ش��������⣺
��1��д�������٩��ܵĹ����У�û���漰���Ļ�ѧ������Ӧ��������Ӧ��������ϡ����û������ֽ⡱�����ֽ⡱֮һ��
��2��С��ͬѧ������pH��ֽ���Բⶨ����Ĵ�����Һ�������ǿ����������ⶨ�ľ��巽���� ��
��3���������£���ʢ��2000g����ʯ��ˮ���ձ�����ε�����������ΪΪ10%��Na2CO3��Һ�����ó�����������������Na2CO3��Һ��������ϵ������ͼ��ʾ��
�ٵ�������ҺNa2CO3 106gʱ����ͼ��A�㣩���ձ�����Һ�ﺬ�е�����Ϊ��д��ѧʽ����
�ڵ�����10%��Na2CO3��Һ150gʱ������B�㣩����ͨ�����㣺���ʱ������Һ�������Ƕ������������ȷ��0.1g��
���𰸡�
��1���û�
��2���ò�����պȡ̼������ҺͿ��pH��ֽ��,����ʾ����ɫ�����ɫ������,����̼������Һ��pH��
��3����������,�μӷ�Ӧ��̼���Ƶ�����Ϊ��106g��10%=10.6g,������̼��Ƶ�����Ϊx
Na2CO3+Ca��OH��2�T | CaCO3��+2NaOH |
106 | 100 |
10.6g | x |
![]() x=10g������10%��Na2CO3��Һ150gʱ,��ʱ������Һ��������2000g+150g��10g=2140g�𣺴�ʱ������Һ��������2140g��
x=10g������10%��Na2CO3��Һ150gʱ,��ʱ������Һ��������2000g+150g��10g=2140g�𣺴�ʱ������Һ��������2140g��
���������⣺��1���Ʊ��ռ�Ĺ��̣�̼��Ƹ��·ֽ����������ƺͶ�����̼����������ˮ���������������ƣ�����������̼���ƽ����ɷ������������ƺ�̼��ƣ����ڸ��ֽⷴӦ��û���漰���û���Ӧ������û�����2����pH��ֽ���Բⶨ����Ĵ�����Һ�������ǿ���ľ�������Ϊ���ò�����պȡ̼������ҺͿ��pH��ֽ�ϣ�����ʾ����ɫ�����ɫ�����գ�����̼������Һ��pH������ò�����պȡ̼������ҺͿ��pH��ֽ�ϣ�����ʾ����ɫ�����ɫ�����գ�����̼������Һ��pH����3���ٵ�������ҺNa2CO3 106gʱ���������ƺ�̼����ǡ����ȫ��Ӧ������Һ�е��������������ƣ�
�����㾫����������Ĺؼ�����������ݻ�ѧ��Ӧ����ʽ�ļ�������֪ʶ�����ո����ʼ�������=ϵ������Է�������֮�ȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�