题目内容
将60g K2CO3溶液与108.7g BaCl2溶液混合,恰好完全反应.过滤后所得滤液的质量为149g.请计算:
(已知:K2CO3+BaCl2=2KCl+BaCO3↓)
(1)反应生成沉淀的质量.
(2)所得滤液中溶质的质量分数.
(3)若将50g 20%的K2CO3溶液稀释成5%的K2CO3溶液,需要水的质量是多少?
(已知:K2CO3+BaCl2=2KCl+BaCO3↓)
(1)反应生成沉淀的质量.
(2)所得滤液中溶质的质量分数.
(3)若将50g 20%的K2CO3溶液稀释成5%的K2CO3溶液,需要水的质量是多少?
考点:根据化学反应方程式的计算,用水稀释改变浓度的方法,有关溶质质量分数的简单计算
专题:有关化学方程式的计算
分析:反应前后的质量差即为生成沉淀碳酸钡的质量,根据碳酸钡的质量可以计算反应生成氯化钾的质量,进一步可以计算所得滤液中溶质的质量分数;溶液稀释前后,溶质质量不变.
解答:解:(1)反应生成的沉淀碳酸钡的质量为:60g+108.7g-149g=19.7g,
答:生成沉淀的质量为19.7g.
(2)设生成氯化钾的质量为x,
K2CO3+BaCl2=2KCl+BaCO3↓,
149 197
x 19.7g
=
,
x=14.9g,
所得滤液中溶质的质量分数为:
×100%=10%,
答:氯化钾的质量分数为:10%.
(3)设需要水的质量为y,
50g×20%=(50g+y)×5%,
y=150g,
答:若将50g20%的K2CO3溶液稀释成5%的K2CO3溶液,需要水的质量是150g.
答:生成沉淀的质量为19.7g.
(2)设生成氯化钾的质量为x,
K2CO3+BaCl2=2KCl+BaCO3↓,
149 197
x 19.7g
| 149 |
| x |
| 197 |
| 19.7g |
x=14.9g,
所得滤液中溶质的质量分数为:
| 14.9g |
| 149g |
答:氯化钾的质量分数为:10%.
(3)设需要水的质量为y,
50g×20%=(50g+y)×5%,
y=150g,
答:若将50g20%的K2CO3溶液稀释成5%的K2CO3溶液,需要水的质量是150g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
质量守恒定律是帮助我们认识化学反应实质的重要理论.在化学反应aA+bB═cC+dD中,下列说法正确的是( )
| A、化学计量数a与b之和一定等于c与d之和 |
| B、若取xg A和xg B反应,生成C和D的质量总和不一定是2xg |
| C、反应物A和B的质量比一定等于生成物C和D的质量比 |
| D、在反应中A、B、C、D四种物质的粒子数目比为a:b:c:d |
 (1)合理使用氮肥、磷肥、钾肥是农业增产的重要手段,下列属于复合肥的是(填序号,下同)
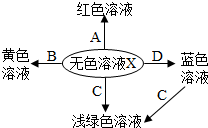
(1)合理使用氮肥、磷肥、钾肥是农业增产的重要手段,下列属于复合肥的是(填序号,下同) 碳元素是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图的转化关系图.请回答下列问题:
碳元素是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图的转化关系图.请回答下列问题:
 小明冬天到仙女山滑雪时用了一盒“自热米饭”,对其中的发热包产生了兴趣:使用时在其表面加入水,就会产生大量热将上层的米饭加热.通过上网查询,了解到发热包的成分有:铁粉、生石灰、碳酸钠、盐、活性炭等.通过已有的化学知识,小明知道:
小明冬天到仙女山滑雪时用了一盒“自热米饭”,对其中的发热包产生了兴趣:使用时在其表面加入水,就会产生大量热将上层的米饭加热.通过上网查询,了解到发热包的成分有:铁粉、生石灰、碳酸钠、盐、活性炭等.通过已有的化学知识,小明知道: