题目内容
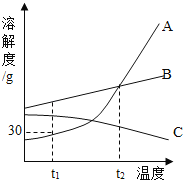
【题目】某一溶液由盐酸、碳酸钠、稀硫酸、氯化铜、氯化钠中的一种或几种混合而成.现向该混合溶液中滴入氢氧化钡溶液,产生的沉淀质量与加入氢氧化钡溶液体积如图所示,则下列判断正确的是( )

A.该溶液中含有硫酸或盐酸,也可能两种酸同时含有
B.该溶液中不可能含碳酸钠
C.该溶液是否含氯化铜不能确定
D.该溶液的组成只可能有一种情况
【答案】B
【解析】根据图象可以看出,加入氢氧化钡溶液而临时没有沉淀产生,所以一定不能含有硫酸根离子,所以不能含有硫酸.所以沉淀不会有硫酸钡.所以对应的沉淀是氢氧化铜,由于开始没有沉淀产生,所以一定含有酸,所以一定是含有盐酸.盐酸的存在导致一定不能同时含有碳酸钠.氯化钠的存在与否无从判断.
A、硫酸只要和氢氧化钡接触,就会生成沉淀,而图象是滴加氢氧化钡一定质量才出现沉淀,所以一定没有硫酸,故A错误,
B、开始加入的一定时间无沉淀,是在中和氢氧化钡,所以一定存在盐酸.盐酸和碳酸钠不能共存,一定不存在碳酸钠,故B正确,
C、由于排除了硫酸和碳酸钠,要出现沉淀只有氢氧化钡和氯化铜反应生成氢氧化铜沉淀,所以一定存在氯化铜,故C错误,
D、对于氯化钠的存在对现象不影响,所以可能存在,也可能不存在,就不是只有一种情况,故D错误,
故选B.

【题目】一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.

(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是 ;
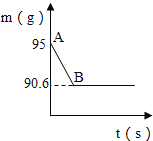
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
样品质量 | 反应前总质量 | 反应后总质量 |
10.6克 | 148.5克 | 146.3克 |
计算生成二氧化碳的质量及该样品中Na2CO3的质量分数.
(3)有图可以判断,在该样品溶液中加入稀盐酸,首先与之反应的物质是 .