题目内容
(4分)K2Cr2O7(重铬酸钾)和KMnO4是重要的化学试剂。
(1) K2Cr2O7中铬元素的化合价是 ,硫酸铬(铬元素为+3价)的化学式为 。
(2) KMnO4是 色的固体,它可用于制取氯气,发生反应的化学方程式为:2KMnO4 + 16HCl =" 2KCl" + 2X + 5Cl2↑+ 8H2O,请写出X物质的化学式 。
(1) K2Cr2O7中铬元素的化合价是 ,硫酸铬(铬元素为+3价)的化学式为 。
(2) KMnO4是 色的固体,它可用于制取氯气,发生反应的化学方程式为:2KMnO4 + 16HCl =" 2KCl" + 2X + 5Cl2↑+ 8H2O,请写出X物质的化学式 。
(1) +6 Cr2(SO4)3 (2) 暗紫 MnCl2
(1)K2Cr2O7中,K元素的化合价为+1价,O元素的化合价为-2价,设该化合物中Cr元素的化合价为x,根据化合物中正负化合价的代数和为0,则
(+1)×2+x×2+(-2)×7=0 解得x=+6
根据化合价书写物质的化学式,可以根据“正左负右标上价,交叉约简写右下”来书写,硫酸根为-2价,铬元素为+3价,故化学式为Cr2(SO4)3;
(2)KMnO4为暗紫色固体,根据质量守恒定律可知,反应前后各原子的种类与数目不变,反应前2KMnO4 和16HCl共有2个钾原子、2个锰原子、8个氧原子、16个氢原子和16个氯原子,反应后2KCl 、5Cl2和 8H2O已有2个钾原子、12个氯原子、8个氢原子和8个氧原子,故2X应含有2个锰原子和4个氯原子,故X的化学式为MnCl2。
(+1)×2+x×2+(-2)×7=0 解得x=+6
根据化合价书写物质的化学式,可以根据“正左负右标上价,交叉约简写右下”来书写,硫酸根为-2价,铬元素为+3价,故化学式为Cr2(SO4)3;
(2)KMnO4为暗紫色固体,根据质量守恒定律可知,反应前后各原子的种类与数目不变,反应前2KMnO4 和16HCl共有2个钾原子、2个锰原子、8个氧原子、16个氢原子和16个氯原子,反应后2KCl 、5Cl2和 8H2O已有2个钾原子、12个氯原子、8个氢原子和8个氧原子,故2X应含有2个锰原子和4个氯原子,故X的化学式为MnCl2。

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
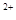 中数字“2”的含义_________________________________________________
中数字“2”的含义_________________________________________________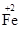 O 数字“2”的含义 ___________________________________________________
O 数字“2”的含义 ___________________________________________________