题目内容
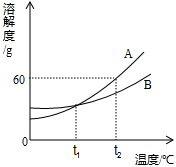
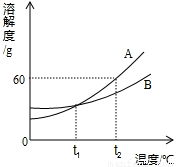
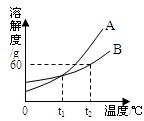 18、(I)如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
18、(I)如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:(1)A、B两种物质的溶解度受温度影响较大的是
A
;(2)t1℃时,A物质的溶解度
=
B物质的溶解度(填“>”、“=”或“<”);t2℃时,把80g B物质放入100g水中,充分搅拌,得到溶液的质量160
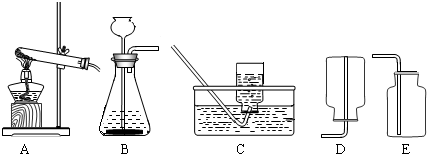
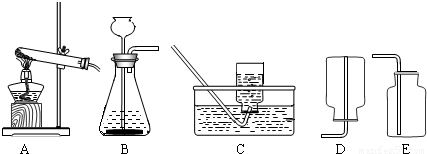
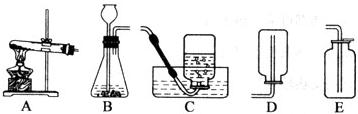
g.(II)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
(1)现选择合适的装置来制取并收集NH3,应该选择的发生装置是
A
,收集装置是D
.(2)若用湿润的红色石蕊试纸来检验NH3,产生的现象是
湿润的红色石蕊试纸变蓝
.
(III)工业上采用氨氧化法制硝酸,该工业生产的第一步反应为4NH3+5O2=4X+6H2O,则X的化学式为
NO
.分析:(I)利用溶解度曲线,分析溶解度受温度影响的大小、比较物质溶解度的大小及物质溶解情况.曲线“坡度”大溶解度受温度影响大;曲线在上方的物质溶解度大于曲线处于下方的物质;一定温度下一定量的溶剂溶解溶质有最大值.
(II)根据气体制取原理反应及气体性质,选择制取气体的装置及气体的检验.发生装置考虑反应物的状态和反应条件;收集装置的选择:密度大于空气用向上排气法,密度小于空气用向下排气法,不溶于水用排水法;呈碱性的气体能使湿润的红色石蕊试纸变蓝.
(III)利用质量守恒定律,推断反应中未知物质的化学式.化学变化前后,原子的种类和个数不变.
(II)根据气体制取原理反应及气体性质,选择制取气体的装置及气体的检验.发生装置考虑反应物的状态和反应条件;收集装置的选择:密度大于空气用向上排气法,密度小于空气用向下排气法,不溶于水用排水法;呈碱性的气体能使湿润的红色石蕊试纸变蓝.
(III)利用质量守恒定律,推断反应中未知物质的化学式.化学变化前后,原子的种类和个数不变.
解答:解:(I)(1)A的溶解度曲线坡度大于B,所以A物质的溶解度受温度影响较大.
故选A;
(2)t1℃时,两条曲线相交于一点,说明此时两物质的溶解度相等.
故答:=;
t2℃时,B的溶解度为60g,此时100g只能溶解60gB物质,所以,t2℃时,把80g B物质放入100g水中,充分搅拌后有20gB未被溶解.所得溶液质量为100g+60g=160g.
故答:160;
(II)(1)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,所以发生装置应选A;NH3极易溶于水,密度比空气小.所以收集氨应选择向下排气法收集,即选D装置.
故选A,D;
(2)NH3极易溶于水,其水溶液呈碱性,能使湿润的红色石蕊试纸变蓝.
故答:湿润的红色石蕊试纸变蓝;
(III)根据质量守恒定律,化学变化前后,原子的种类和个数不变,可推断反应中生成物4X应含有4个N原子和4个O原子,所以X的化学式为NO.
故答:NO.
故选A;
(2)t1℃时,两条曲线相交于一点,说明此时两物质的溶解度相等.
故答:=;
t2℃时,B的溶解度为60g,此时100g只能溶解60gB物质,所以,t2℃时,把80g B物质放入100g水中,充分搅拌后有20gB未被溶解.所得溶液质量为100g+60g=160g.
故答:160;
(II)(1)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,所以发生装置应选A;NH3极易溶于水,密度比空气小.所以收集氨应选择向下排气法收集,即选D装置.
故选A,D;
(2)NH3极易溶于水,其水溶液呈碱性,能使湿润的红色石蕊试纸变蓝.
故答:湿润的红色石蕊试纸变蓝;
(III)根据质量守恒定律,化学变化前后,原子的种类和个数不变,可推断反应中生成物4X应含有4个N原子和4个O原子,所以X的化学式为NO.
故答:NO.
点评:考题涉及三个部分的内容,且互不相关,在解答此类综合型考题时注意把知识点分开进行思考.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

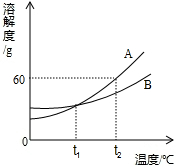 (I)如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
(I)如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题: