题目内容
【题目】原子结构与元素的性质和物质的组成密切相关,请将答案填写在下面的横线上:
(1)镁原子的结构示意图为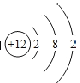 ,其在化学反应中易_________(填“得到”或“失去”)电子,其离子符号是________。
,其在化学反应中易_________(填“得到”或“失去”)电子,其离子符号是________。
(2)钠元素与氯元素组成的化合物是_________(化学式),构成该物质的微粒是_______(选填“分子”、“原子”、或“离子”);
(3)与元素化学性质关系最密切的是_________(填字母编号);
A. 元素的相对原子质量 B. 元素的核电荷数
C. 原子的核外电子数 D. 原子的最外层电子数
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是_______(填字母编号)。
A. 构成它们的原子大小不同 B. 构成它们的原子数目不同
C. 金刚石、石墨由不同种原子组成 D. 金刚石、石墨里碳原子排列方式不同
(5)铅元素相关信息如图所示。下列说法中正确的是(_______)
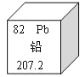
A.铅原子核内有82个电子 B.相对原于质量为207. 2 g
C.铅有毒,儿童不能使用铅笔 D.铅可与稀硫酸反应,产生氢气
【答案】失去 Mg2+ NaCl 离子 D D A
【解析】
(1)由镁的原子结构示意图,最外层电子数是2,在化学反应中易失去2个电子而形成阳离子,其离子符号为:Mg2+;
(2)钠元素与氯元素组成的化合物是氯化钠,化学式是NaCl,构成该物质的微粒是离子;
(3)由题意可知,最外层电子数与元素的化学性质关系最密切.因为物质参加化学反应时发生作用(得失电子)的一般只是最外层电子;
(4)由于金刚石和石墨中碳原子的排列方式不同造成了金刚石和石墨物理性质具有很大差异;
(5)A、根据铅元素相关信息可知,原子序数=质子数=核外电子数=82,故正确;
B、相对原子质量的单位不是“g”而是“1”,通常省略,故错误;
C、铅笔芯是用石墨制成的,不含铅,故错误;
D、排在金属活动性顺序表氢前的金属可与酸发生反应生成氢气,根据图示信息无法判断铅是否排在金属活动性顺序表的前面,故错误。

 阅读快车系列答案
阅读快车系列答案【题目】已知化学反应X+Y=Z,现进行了两次实验,测得数据如表所示:
实验序号 | 反应物的质量/g | 产物Z的质量/g | |
X | Y | ||
① | 9.0 | 1.6 | 9.6 |
② | 5.0 | 2.4 | 6.0 |
若将①和②的反应物全部混合在一起,最多可生成产物Z( )
A. 16.6g B. 16.8g C. 17.0g D. 15.6g