题目内容
为了降低城乡居民因食物和饮用水中含碘量不足而导致碘缺乏症的发病率,我国已执行食盐加碘的法规,下表是某地市售二级碘盐的商品包装袋上的部分文字说明.请根据此表,结合所学的相关知识,回答下列问题:
| 配料表 | 精制海盐、碘酸钾 |
| 氯化钠含量 | 94% |
| 含碘量 | (20~40)mg/kg |
| 食用方法 | 待食物烹调好后再放入碘盐,勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
(2)1000g碘盐中约含碘20mg.这里标明的碘的含量是指________
A.碘单质 B.碘元素 C.碘原子 D.碘分子
(3)已知碘酸钾的化学式为KIO3,请列式计算:(K-39 I-127 O-16)
①碘酸钾的相对分子质量;
②碘酸钾中碘元素的质量分数. (结果保留小数点后一位小数)
(4)若一包食盐质量为1000g,其中含KIO35%,则这包食盐中含碘元素多少克?
解:(1)食用方法和贮藏指南可推测碘酸钾的化学性质有碘酸钾受热或见光时化学性质不稳定,易分解或在潮湿的空气中易受潮;
(2)这里标明的碘的含量是指碘元素;
(3)①碘酸钾的相对分子质量=39+127+16×3=214;
②碘酸钾中碘元素的质量分数=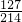 ×100%=59.3%;
×100%=59.3%;
(4)碘酸钾的质量=1000g×5%=50g.碘元素的质量=50g×59.3%=29.65g.
故答案为:
(1)碘酸钾受热或见光时化学性质不稳定,易分解或在潮湿的空气中易受潮;(2)B;(3)①214;②59.3%(4)29.65g.
分析:(1)根据食用方法和贮藏指南可推测碘酸钾的化学性质有碘酸钾受热或见光时化学性质不稳定,易分解或在潮湿的空气中易受潮进行解答;
(2)根据这里标明的碘的含量是指碘元素进行解答;
(3)根据碘酸钾的相对分子质量为各原子的相对原子质量总和以及碘酸钾中碘元素的质量分数= 进行解答;
进行解答;
(4)根据碘酸钾的含量以及碘酸钾中碘元素的质量分数进行解答.
点评:本题主要考查盐的概念,解答时要分析各种物质的组成,然后再根据盐概念的含义进行分析、判断,从而得出正确的结论.同时要善于从说明中总结物质的性质.
(2)这里标明的碘的含量是指碘元素;
(3)①碘酸钾的相对分子质量=39+127+16×3=214;
②碘酸钾中碘元素的质量分数=
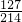 ×100%=59.3%;
×100%=59.3%;(4)碘酸钾的质量=1000g×5%=50g.碘元素的质量=50g×59.3%=29.65g.
故答案为:
(1)碘酸钾受热或见光时化学性质不稳定,易分解或在潮湿的空气中易受潮;(2)B;(3)①214;②59.3%(4)29.65g.
分析:(1)根据食用方法和贮藏指南可推测碘酸钾的化学性质有碘酸钾受热或见光时化学性质不稳定,易分解或在潮湿的空气中易受潮进行解答;
(2)根据这里标明的碘的含量是指碘元素进行解答;
(3)根据碘酸钾的相对分子质量为各原子的相对原子质量总和以及碘酸钾中碘元素的质量分数=
 进行解答;
进行解答;(4)根据碘酸钾的含量以及碘酸钾中碘元素的质量分数进行解答.
点评:本题主要考查盐的概念,解答时要分析各种物质的组成,然后再根据盐概念的含义进行分析、判断,从而得出正确的结论.同时要善于从说明中总结物质的性质.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目