题目内容
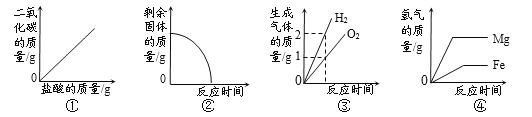
【题目】某工厂废水中含碳酸钠(易溶于水),造成水体污染。化学兴趣小组设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示。请回答下列问题(碳酸钠与盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,不考虑水样中杂质的影响):
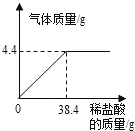
(1)反应生成CO2气体的质量是_____g;
(2)求废水中碳酸钠的质量分数。____(写出计算过程)
【答案】4.4g 5.3%
【解析】
解:设废水中碳酸钠的质量分数为x
由图可知,生成的二氧化碳的质量为4.4g
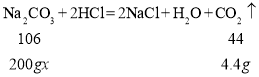
![]()
x=5.3%
答:(1)反应生成CO2气体的质量是 4.4g;
(2)废水中碳酸钠的质量分数为5.3%。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
【题目】一密闭容器中有甲、乙、丙、丁四种物质,在一定条件下发生化学反应.一段时间后,测得反应前后各物质质量如下表.下列说法正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前物质的质量/g | 4 | 16 | 6 | 2 |
反应后物质的质量/g | 8 | 1 | x | 12 |
A. 反应不遵守质量守恒定律
B. 甲为反应物,乙为生成物,丙可能是该反应的催化剂
C. 参加反应的乙和丁的质量比为2:3
D. 已知甲和丁的化学式量之比为2:5,则方程式中甲与丁的化学计量数之比为1:1