题目内容
【题目】铅蓄电池在生产、生活中使用广泛,其构造如图所示。
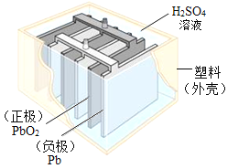
(1)铅蓄电池充电时是将电能转化为_____(填序号)
a.机械能 b.热能 c.化学能
(2)铅蓄电池的工作原理可以表示为:2PbSO4+2H2O![]() Pb+PbO2+2H2SO4。据此可知,铅蓄电池在放电时,溶液pH将不断填_____(“增大”“减小”或“不变”)。
Pb+PbO2+2H2SO4。据此可知,铅蓄电池在放电时,溶液pH将不断填_____(“增大”“减小”或“不变”)。
(3)从材料分类角度看,塑料属于_____材料。
(4)废硫酸直接排放会污染环境,用石灰浆处理废硫酸的化学方程式是_____。
【答案】c 增大 合成(合理即可) Ca(OH)2+H2SO4═CaSO4+2H2O
【解析】
(1)铅蓄电池充电时是将电能转化为化学能,故选c;
(2)由铅蓄电池的总反应PbO2+2H2SO4+Pb![]() 2PbSO4+2H2O可知,铅蓄电池放电时硫酸被消耗,所以酸性减弱,pH不断增大;
2PbSO4+2H2O可知,铅蓄电池放电时硫酸被消耗,所以酸性减弱,pH不断增大;
(3)塑料属于有机合成材料;
(4)氢氧化钙与硫酸发生中和反应生成硫酸钙和水,反应方程式为Ca(OH)2+H2SO4═CaSO4+2H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
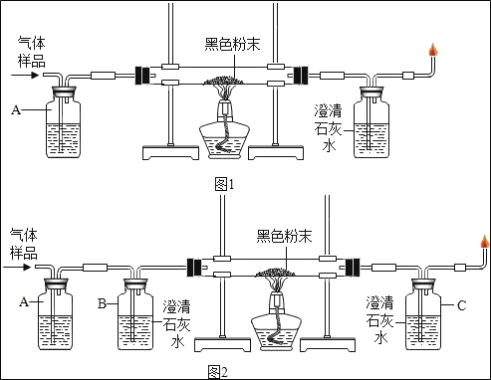
小学生10分钟应用题系列答案【题目】干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质。某研究 小组对一只干燥管里的碱石灰样品的成分进行实验探究。
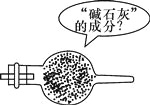
(提出猜想) 猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠; 猜想Ⅱ:已经变质,可能情况未知;猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠;
(实验探究)
(1)取样品,加入几滴清水,试管外壁不发烫;
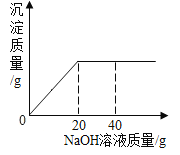
(2)取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀和红色滤液;
(分析过程)
根据实验(1)说明猜想_____(填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。根据实 验(2)甲同学认为猜想Ⅲ成立,乙同学不同意,他认为碱石灰样品中不一定含有碳酸钙, 可能含有氢氧化钙,他的理由是_________(请写化学方程式)。
为进一步确定猜想,他们设计了以下实验方案:
实验方案 | 实验现象 | 分析 |
①取红色滤液,通入一定_____ 量的 CO2 气体 | 若产生_______ | 滤液中含有 Ca(OH)2 |
②取红色滤液,加入过量 的_____溶液 | 若产生白色沉淀,溶液仍然呈红色 | 滤液中含有_______ |
若产生白色沉淀,溶液呈无色 | 滤液中只含 Na2CO3 |
(实验结论)甲、乙同学完成设计的实验方案后,证明了猜想Ⅱ成立。
(实验反思)根据上述实验,下列说法正确的是_____(填序号)。
A 过滤后得到的红色滤液中的溶质只有 3 种可能的组合
B 表格中的方案①,若通入的 CO2 适量,溶液可能由红色变成无色
C 实验证明了原碱石灰样品中一定不含 CaCO3
D 根据实验可知,碱石灰样品的变质情况有 2 种可能性