题目内容
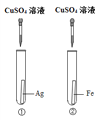
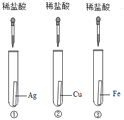
为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。请从两个方案中任选1个作答,若两个均作答,按方案A计分。
方案A | 方案B |
|
|
(1)实验中发生反应的化学方程式为______。 (2)实验中观察到的现象是______。 (3)该方案______(填“能”或“不能”)验证三种金属的活动性。 | (1)实验中发生反应的化学方程式为______。 (2)实验中观察到的现象是______。 (3)该方案______(填“能”或“不能”)验证三种金属的活动性。 |
练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目



 稀释浓硫酸 B.
稀释浓硫酸 B.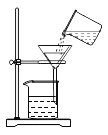 过滤
过滤 点燃酒精灯 D.
点燃酒精灯 D. 称量NaCl固体
称量NaCl固体 填写健康申报卡 B.
填写健康申报卡 B. 每天用消毒剂进行教室消毒
每天用消毒剂进行教室消毒 入校扫描云南健康码 D.
入校扫描云南健康码 D. 一日三次用体温计测体温
一日三次用体温计测体温