题目内容
某化学兴趣小组的同学对一份固体样品进行了探究.通过实验已确定该样品由氧化铁和铁粉混合而成.他们称取了13.6g固体样品,用图甲所示的装置继续实验,测定的部分数据如图乙所示.
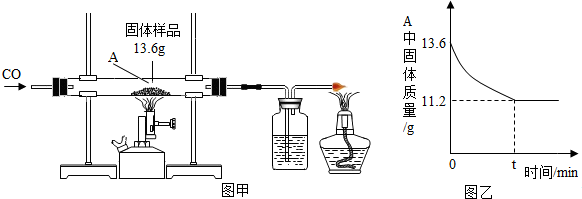
请计算:
(1)固体样品中氧化铁的质量是 g;
(2)在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数.

请计算:
(1)固体样品中氧化铁的质量是
(2)在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据一氧化碳只与氧化铁反应,写出化学反应式,根据提供的数据计算出氧化铁的质量;
(2)根据铁和稀盐酸反应的化学方程式,利用铁的质量计算出生成的溶质氯化亚铁和氢气的质量,根据质量守恒定律计算出溶液的质量,然后根据质量分数公式计算即可.
(2)根据铁和稀盐酸反应的化学方程式,利用铁的质量计算出生成的溶质氯化亚铁和氢气的质量,根据质量守恒定律计算出溶液的质量,然后根据质量分数公式计算即可.
解答:解:(1)设氧化铁的质量为x,则
3CO+Fe2O3
2Fe+3CO2 固体减重
160 112 160-112=48
x (13.6g-11.2 g)
=
解得x=8g
(2)设生成的FeCl2和H2质量分别为x、y,则
Fe+2HCl=FeCl2+H2↑
56 127 2
11.2g x y
=
,
=
解得x=25.4g; y=0.4g
所得溶液中溶质的质量分数为
×100%=22.9%.
答:(1)8;(2)所得溶液中溶质的质量分数为22.9%.
3CO+Fe2O3
| ||
160 112 160-112=48
x (13.6g-11.2 g)
| 160 |
| x |
| 48 |
| 13.6g-11.2g |
解得x=8g
(2)设生成的FeCl2和H2质量分别为x、y,则
Fe+2HCl=FeCl2+H2↑
56 127 2
11.2g x y
| 56 |
| 11.2g |
| 127 |
| x |
| 56 |
| 11.2g |
| 2 |
| y |
解得x=25.4g; y=0.4g
所得溶液中溶质的质量分数为
| 25.4g |
| 11.2g+100g-0.4g |
答:(1)8;(2)所得溶液中溶质的质量分数为22.9%.
点评:本题考查关于化学反应式的计算,需要同学们能够准确的书写化学反应式,理清物质间的关系,才可做出准确的计算.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
下列化学实验基本操作中正确的是( )
A、 |
B、 |
C、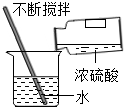 |
D、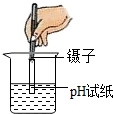 |
推理是化学学习中常用的思维方法,以下推理正确的是( )
| A、盐酸和硫酸能使石蕊试液变红,碳酸也能使石蕊试液变红 |
| B、氢气和氧气可以用排水法收集,二氧碳也可以用排水法收集 |
| C、氢氧化钠和氢氧化钙能与二氧化碳反应,氢氧化镁也能与二氧化碳反应 |
| D、铁和镁都能与稀盐酸反应,铜也能与稀盐酸反应 |
二氧化碳和氧气是自然界中生命活动不可缺少的两种气体,它们的相同点是( )
| A、都能灭火 |
| B、都是光合作用的原料 |
| C、都能供呼吸 |
| D、都无毒 |