题目内容
下列四个图象中正确的是
- A.
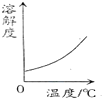
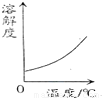
氧气在水中的溶解度随温度变化图 - B.
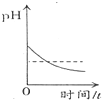
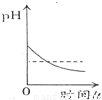
治疗胃酸过多时胃液PH随时间变化图 - C.
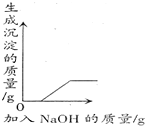
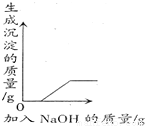
向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量 - D.
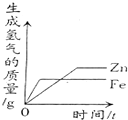
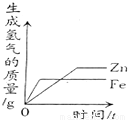
常温下,相同质量的锌和铁分别与足量质量分数相同的稀硫酸反应
C
分析:A、根据气体的溶解度与温度的关系考虑;B、根据胃酸的pH值考虑;C、根据酸碱反应优先的原则考虑;D、根据金属铁和锌的活泼性和等质量金属与足量硫酸反应生成氢气质量的多少考虑.
解答:A、气体的溶解度与温度成反比,随着温度的升高而减小,故A错;
B、治疗胃酸过多时,应该加入碱性药品,在没加入药品前,胃酸是盐酸,所以胃液PH应该小于7,图示则大于7,故B错;
C、向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液,氢氧化钠先与硫酸反应生成硫酸钠和水,所以开始没有沉淀生成,当把硫酸反应完,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,开始产生沉淀,反应完毕,不再产生沉淀,就改成横线了;
D、由于锌比铁活泼,所以锌先到达最高点,由于等质量的锌和铁与足量硫酸反应,铁生成氢气的质量要大于锌生成氢气的质量,所以铁的曲线在上边,锌的曲线在下边,故D错.
故选C.
点评:本题容易出错的地方是C答案,由于氢氧化钠与硫酸铜反应生成的氢氧化铜沉淀,虽然不溶于水,但能溶于酸,所以有硫酸存在就不会产生沉淀,只有把硫酸反应完才能产生氢氧化铜沉淀.
分析:A、根据气体的溶解度与温度的关系考虑;B、根据胃酸的pH值考虑;C、根据酸碱反应优先的原则考虑;D、根据金属铁和锌的活泼性和等质量金属与足量硫酸反应生成氢气质量的多少考虑.
解答:A、气体的溶解度与温度成反比,随着温度的升高而减小,故A错;
B、治疗胃酸过多时,应该加入碱性药品,在没加入药品前,胃酸是盐酸,所以胃液PH应该小于7,图示则大于7,故B错;
C、向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液,氢氧化钠先与硫酸反应生成硫酸钠和水,所以开始没有沉淀生成,当把硫酸反应完,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,开始产生沉淀,反应完毕,不再产生沉淀,就改成横线了;
D、由于锌比铁活泼,所以锌先到达最高点,由于等质量的锌和铁与足量硫酸反应,铁生成氢气的质量要大于锌生成氢气的质量,所以铁的曲线在上边,锌的曲线在下边,故D错.
故选C.
点评:本题容易出错的地方是C答案,由于氢氧化钠与硫酸铜反应生成的氢氧化铜沉淀,虽然不溶于水,但能溶于酸,所以有硫酸存在就不会产生沉淀,只有把硫酸反应完才能产生氢氧化铜沉淀.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目