题目内容
从事科学实验的重要环节是进行科学实验设计.科学实验的正确步骤应为:①明确实验目的;②收集有关资料;③设计合理方案;④进行科学实验.请你按照以上四个步骤,完成以下实验设计,根据图回答问题: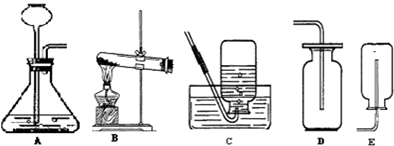
(1)在实验室中用过氧化氢(H2O2)制取氧气.
[明确实验目的]:用过氧化氢在实验室里制取氧气.
[收集有关资料]过氧化氢是一种无色液体,在二氧化锰的催化作用下,迅速分解出氧气,其反应的文字表达式或化学方程式为:________.
[设计合理方案]:发生装置选用________(填序号,下同),收集装置选用________.
[进行科学实验]
①分液漏斗中应放入的物质是________,锥形瓶中应放入的物质是________.
②要收集一瓶纯净的氧气应选择图中的装置________(填字母)
③某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因是________.
④若实验时用此法代替高锰酸钾加热制氧气,优点是________(填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
⑤装置A中反应剧烈,据此提出实验安全注意事项是________
A.改用分液漏斗控制液体的滴加速度 B.用体积小的锥形瓶 C.加热反应物
(2)在实验室中,可以用加热氯酸钾(KClO3)和二氧化锰固体混合物制取氧气.
①[明确实验目的]:________.
②[收集有关资料]:氯酸钾是白色的固体,二氧化锰是黑色的固体.且二氧化锰在反应中________.反应原理(表达式)________;
③设计合理方案:发生装置选用________,若选用D收集装置收集氧气,你验证集气瓶中是否已收集满的方法是________.
解:(1)过氧化氢制氧气的反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,所以反应方程式为:2H2O2 2H2O+O2↑
2H2O+O2↑
(或文字表达式:过氧化氢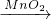 水+氧气);
水+氧气);
用过氧化氢制取氧气是固体与液体,不需要加热,所以发生装置是A,氧气不易溶于水且密度比空气大,所以可以用C或D来收集;
①过氧化氢溶液从长颈漏斗口加入,二氧化锰从锥形瓶口加入;
②排空气法和排水法相对来说,排水法收集的气体更纯;
③根据观察到锥形瓶内有大量气泡产生,说明反应产生了氧气;但开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃,说明气体溢出了,装置漏气;
④根据两种方法的反应条件,可知用过氧化氢溶液分解不需要加热,操作就比较简单;产物都不止一种,故选择B;
⑤装置A中反应剧烈,说明可能是反应物浓度太大或滴加速度太快,而分液漏斗可以控制液体滴加的速度;用体积小的锥形瓶不会改变反应速度;加热会加快反应;故选择:A;
(2)①通过下面的收集资料就能判断实验目的是:用氯酸钾制取氧气;
②催化剂所起的作用叫催化作用;反应的方程式为:2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
③固体与固体制取气体需要加热,所以发生装置选择B,因为氧气能使带火星的木条复燃,所以用带火星的木条来验满,放到瓶口能复燃说明满了,否则不满.
故答案为:(1)2H2O2 2H2O+O2↑(或过氧化氢
2H2O+O2↑(或过氧化氢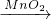 水+氧气);A;C或D;①过氧化氢溶液 二氧化锰; ②C; ③装置漏气;④B;⑤A;
水+氧气);A;C或D;①过氧化氢溶液 二氧化锰; ②C; ③装置漏气;④B;⑤A;
(2)①用加热氯酸钾(KClO3)和二氧化锰固体混合物制取氧气;②起催化作用;2KClO3 2KCl+3O2↑;③B;用带火星的木条放到集气瓶口,看是否熄灭.
2KCl+3O2↑;③B;用带火星的木条放到集气瓶口,看是否熄灭.
分析:(1)过氧化氢在二氧化锰的作用下分解成水和氧气,写出其反应方程式;根据反应物的状态和反应条件选择发生装置;根据气体的密度和溶解性选择收集装置;
①固体一般从锥形瓶口加入,液体从长颈漏斗口加入;②排空气法和排水法相对来说,排水法收集的气体更纯;③装置漏气就收集不到气体;④根据操作的简单性及生成的产物分析;⑤根据分液漏斗的作用分析;
(2)①实验目的要根据下面的步骤去推并模仿(1)来写;②根据催化剂的作用回答;③氯酸钾制氧气需要加热,根据氧气能使带火星的木条复燃的特性来验满.
点评:通过本题学生进一步明确了科学实验的正确步骤,通过分析本题加深了气体收集方法的选取方法,发生装置的选择方法,氧气的验满方法等.
 2H2O+O2↑
2H2O+O2↑(或文字表达式:过氧化氢
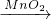 水+氧气);
水+氧气);用过氧化氢制取氧气是固体与液体,不需要加热,所以发生装置是A,氧气不易溶于水且密度比空气大,所以可以用C或D来收集;
①过氧化氢溶液从长颈漏斗口加入,二氧化锰从锥形瓶口加入;
②排空气法和排水法相对来说,排水法收集的气体更纯;
③根据观察到锥形瓶内有大量气泡产生,说明反应产生了氧气;但开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃,说明气体溢出了,装置漏气;
④根据两种方法的反应条件,可知用过氧化氢溶液分解不需要加热,操作就比较简单;产物都不止一种,故选择B;
⑤装置A中反应剧烈,说明可能是反应物浓度太大或滴加速度太快,而分液漏斗可以控制液体滴加的速度;用体积小的锥形瓶不会改变反应速度;加热会加快反应;故选择:A;
(2)①通过下面的收集资料就能判断实验目的是:用氯酸钾制取氧气;
②催化剂所起的作用叫催化作用;反应的方程式为:2KClO3
 2KCl+3O2↑;
2KCl+3O2↑;③固体与固体制取气体需要加热,所以发生装置选择B,因为氧气能使带火星的木条复燃,所以用带火星的木条来验满,放到瓶口能复燃说明满了,否则不满.
故答案为:(1)2H2O2
 2H2O+O2↑(或过氧化氢
2H2O+O2↑(或过氧化氢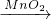 水+氧气);A;C或D;①过氧化氢溶液 二氧化锰; ②C; ③装置漏气;④B;⑤A;
水+氧气);A;C或D;①过氧化氢溶液 二氧化锰; ②C; ③装置漏气;④B;⑤A;(2)①用加热氯酸钾(KClO3)和二氧化锰固体混合物制取氧气;②起催化作用;2KClO3
 2KCl+3O2↑;③B;用带火星的木条放到集气瓶口,看是否熄灭.
2KCl+3O2↑;③B;用带火星的木条放到集气瓶口,看是否熄灭.分析:(1)过氧化氢在二氧化锰的作用下分解成水和氧气,写出其反应方程式;根据反应物的状态和反应条件选择发生装置;根据气体的密度和溶解性选择收集装置;
①固体一般从锥形瓶口加入,液体从长颈漏斗口加入;②排空气法和排水法相对来说,排水法收集的气体更纯;③装置漏气就收集不到气体;④根据操作的简单性及生成的产物分析;⑤根据分液漏斗的作用分析;
(2)①实验目的要根据下面的步骤去推并模仿(1)来写;②根据催化剂的作用回答;③氯酸钾制氧气需要加热,根据氧气能使带火星的木条复燃的特性来验满.
点评:通过本题学生进一步明确了科学实验的正确步骤,通过分析本题加深了气体收集方法的选取方法,发生装置的选择方法,氧气的验满方法等.

练习册系列答案
相关题目