题目内容
(2004?南京)如图所示,实验装置:
(1)写出图中指定仪器的名称:①______;②______;③______;④______.
(2)A装置可用于(填一个具体实验名称,下同)______的实验.
B装置可用于______的实验.
(3)现有稀H2SO4、CuO、Fe粉3种物质,请设计两种制取铜的实验方案.填写下表.
| 实验方案 | 有关反应的化学方程式 | 选用装置(填字母代号) |
| 方案一 | ①______ ②______ |
【答案】分析:(1)根据化学常用仪器的名称进行对比解答.
(2)根据使用A、B装置的反应物的条件分析解答.
(3)根据题中所给反应物和要制备的物质分析反应原理.
(4)根据所给的反应物和要制取的物质来确定反应装置.
解答:解:(1)对照常用仪器的图示及名称,故答案为:①试管,②铁架台,⑧烧杯,④漏斗.
(2)应用A装置应当是固体与固体反应且需加热的实验,故答案为:加热氯酸钾与二氧化锰的混合物制取氧气
B装置应当是固体与液体反应不用加热的实验,故答案为:锌与稀硫酸(稀盐酸)反应制取氢气
(3)反应物有铁、硫酸、氧化铜,可以设计两种方案,①先用硫酸和铁制得氢气,再用氢气还原氧化铜制取铜,需要有制气装置和加热还原装置;②用氧化铜与硫酸反应制得硫酸铜,再用铁置换出硫酸铜中的铜,需要有反应装置和过滤装置,
故答案为:
(4)该反应过程包括了:水和氧化钙制得氢氧化钙,氢氧化钙和碳酸钠反应制得氢氧化钠,该制取过程用到了反应装置,过滤装置,以及蒸发结晶装置,故答案为:DEF.
点评:本题主要考查了由装置设计实验,以及由反应物生成物设计反应原理,综合性较强.
(2)根据使用A、B装置的反应物的条件分析解答.
(3)根据题中所给反应物和要制备的物质分析反应原理.
(4)根据所给的反应物和要制取的物质来确定反应装置.
解答:解:(1)对照常用仪器的图示及名称,故答案为:①试管,②铁架台,⑧烧杯,④漏斗.
(2)应用A装置应当是固体与固体反应且需加热的实验,故答案为:加热氯酸钾与二氧化锰的混合物制取氧气
B装置应当是固体与液体反应不用加热的实验,故答案为:锌与稀硫酸(稀盐酸)反应制取氢气
(3)反应物有铁、硫酸、氧化铜,可以设计两种方案,①先用硫酸和铁制得氢气,再用氢气还原氧化铜制取铜,需要有制气装置和加热还原装置;②用氧化铜与硫酸反应制得硫酸铜,再用铁置换出硫酸铜中的铜,需要有反应装置和过滤装置,
故答案为:
| 实验方案 | 有关反应的化学方程式 | 选用装置(填字母代号) |
| 方案一 | ①Fe+H2SO4=FeSO4+H2↑ ②H2+CuO  Cu+H2O Cu+H2O | B C |
| 方案二 | ①CuO+H2SO4=CuSO4+H2O ②Fe+CuSO4=FeSO4+Cu | D E |
点评:本题主要考查了由装置设计实验,以及由反应物生成物设计反应原理,综合性较强.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
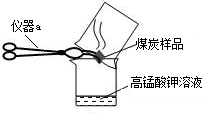
 ”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式:
”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式:


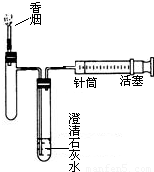 (2004?南京)在今年5月31日世界无烟日宣传活动中,某学生设计了如图所示的实验装置.该装置中的澄清石灰水可以检验香烟燃烧是否有______气体生成.为了使香烟燃烧产生的气体通过澄清石灰水,活塞应向______移动.
(2004?南京)在今年5月31日世界无烟日宣传活动中,某学生设计了如图所示的实验装置.该装置中的澄清石灰水可以检验香烟燃烧是否有______气体生成.为了使香烟燃烧产生的气体通过澄清石灰水,活塞应向______移动.