题目内容
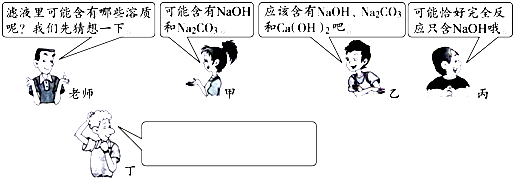
学习碳酸钠知识时,老师做碳酸钠溶液和澄清石灰水反应演示实验,并对浑浊液过滤,得到澄清滤液.课堂上老师的提问和同学们的回答如图所示.
(1)碳酸钠的俗名是
(2)假设你是丁同学,请你提出一个与甲、乙、丙同学不同的猜想,你的猜想是
(3)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的,请说明理由
(4)甲同学针对自己的猜想进行了如下实验:
你认为甲同学的实验设计是否正确?
(5)请你设计实验方案确定滤液中溶质的组成

(1)碳酸钠的俗名是
纯碱
纯碱
.(2)假设你是丁同学,请你提出一个与甲、乙、丙同学不同的猜想,你的猜想是
可能含有NaOH和Ca(OH)2
可能含有NaOH和Ca(OH)2
.(3)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的,请说明理由
乙同学的猜想不合理,因为Na2CO3与Ca(OH)2要发生反应,不可能共存
乙同学的猜想不合理,因为Na2CO3与Ca(OH)2要发生反应,不可能共存
.(4)甲同学针对自己的猜想进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | 猜想不成立 |
不正确
不正确
,其理由是加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在.
加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在.
.(5)请你设计实验方案确定滤液中溶质的组成
取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等
取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等
.分析:碳酸钠和澄清石灰水反应,生成碳酸钙沉淀,同时生成氢氧化钠,所以反应后的滤液里一定含氢氧化钠;物质之间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,但是两种反应物不会同时剩余.碳酸盐的检验是采用加酸观察是否有气体产生的方法,如果是氢氧化钠和碳酸钠共存时,盐酸首先和氢氧化钠反应,然后再与碳酸钠反应.
解答:解:根据化学反应:Na2CO3+Ca(OH)2=CaCO3↓2+NaOH,可以知道,反应后滤液中一定会有氢氧化钠存在,若碳酸钠过量,则含有碳酸钠,即甲同学的猜想,若氢氧化钙过量,则含有氢氧化钙,即丁同学可能提出的猜想,所以本题答案为:可能含有NaOH和Ca(OH)2;
(1)碳酸钠的俗称是纯碱.
(2)若氢氧化钙过量,则含有氢氧化钙,故丁同学的猜想:可能含有NaOH和Ca(OH)2;
(3)物质之间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,但是两种反应物不会同时剩余.所以本题答案为:乙同学的猜想不合理.因为Na2CO3与Ca(OH)2要发生反应,不可能共存.
(4)要证明碳酸钠的存在,涉及到的就是碳酸盐的检验,所以可以采用加酸的方法,但是由于滤液中含有氢氧化钠.需要加入足量的盐酸,仅仅加入几滴盐酸,反应进行的不彻底,不能依据此判断滤液中不含碳酸钠,多以本题答案为:不正确,
理由:加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在.
(5)取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等;
故答案为:
(1)纯碱;
(2)可能含有NaOH和Ca(OH)2;
(3)乙同学的猜想不合理,因为Na2CO3与Ca(OH)2要发生反应,不可能共存;
(4)不正确;加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在;
(5)取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等.
(1)碳酸钠的俗称是纯碱.
(2)若氢氧化钙过量,则含有氢氧化钙,故丁同学的猜想:可能含有NaOH和Ca(OH)2;
(3)物质之间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,但是两种反应物不会同时剩余.所以本题答案为:乙同学的猜想不合理.因为Na2CO3与Ca(OH)2要发生反应,不可能共存.
(4)要证明碳酸钠的存在,涉及到的就是碳酸盐的检验,所以可以采用加酸的方法,但是由于滤液中含有氢氧化钠.需要加入足量的盐酸,仅仅加入几滴盐酸,反应进行的不彻底,不能依据此判断滤液中不含碳酸钠,多以本题答案为:不正确,
理由:加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在.
(5)取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等;
故答案为:
(1)纯碱;
(2)可能含有NaOH和Ca(OH)2;
(3)乙同学的猜想不合理,因为Na2CO3与Ca(OH)2要发生反应,不可能共存;
(4)不正确;加入的盐酸量少,有NaOH存在,就不会有CO2气体放出,但Na2CO3可能存在;
(5)取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应;如果有沉淀出现,说明除氢氧化钠外还含有氢氧化钙或碳酸钠;或者采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠等.
点评:物质之间发生化学反应时会完全进行,存在量的关系,所以不会出现反应物同时剩余的情况.另外在设计实验方案时,为保证实验结果准确,需要控制加入的药品的用量.

练习册系列答案
相关题目
在学习碳酸钠知识时,张老师在做完碳酸钠溶液和澄清石灰水反应演示实验后,对浑浊液过滤,得到澄清的滤液.对于滤液的组成,课堂上老师的提问和同学们的回答如下表:
| 人 员 | 对 话 |
| 老 师 | 问:滤液里可能含有哪些溶质呢? |
| 甲同学 | 答:可能是NaOH、Na2C03 |
| 乙同学 | 答:可能是NaOH、Na2C03、Ca(OH)2 |
| 丙同学 | 答:可能是NaOH |
| 丁同学 | 答:可能是______ |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,______ | ______ | 自己的猜想成立 |
(3)甲同学针对自己的猜想进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入足量稀盐酸 | 没有气体产生 | 甲的猜想不成立 |
(4)为了进一步证明甲同学的猜想,丁同学又进行了又下实验探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,再滴入氯化钙溶液 | 生成______ | 甲的猜想成立 |
在学习碳酸钠知识时,张老师在做完碳酸钠溶液和澄清石灰水反应演示实验后,对浑浊液过滤,得到澄清的滤液.对于滤液的组成,课堂上老师的提问和同学们的回答如下表:
(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在上面表格中.并对你自己的猜想设计一个简单的实验加以证明.
(2)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由.______.
(3)甲同学针对自己的猜想进行了如下实验:
你认为甲同学的实验设计是否正确?请说明理由是______.
(4)为了进一步证明甲同学的猜想,丁同学又进行了又下实验探究:
写出碳酸钠溶液与氯化钙溶液反应的化学方程式______.
| 人 员 | 对 话 |
| 老 师 | 问:滤液里可能含有哪些溶质呢? |
| 甲同学 | 答:可能是NaOH、Na2C03 |
| 乙同学 | 答:可能是NaOH、Na2C03、Ca(OH)2 |
| 丙同学 | 答:可能是NaOH |
| 丁同学 | 答:可能是______ |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,______ | ______ | 自己的猜想成立 |
(3)甲同学针对自己的猜想进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入足量稀盐酸 | 没有气体产生 | 甲的猜想不成立 |
(4)为了进一步证明甲同学的猜想,丁同学又进行了又下实验探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,再滴入氯化钙溶液 | 生成______ | 甲的猜想成立 |