题目内容
(2010?平南县二模)将铁片投入下列溶液中放置一段时间后,溶液质量增大的是( )
分析:根据物质间的反应进行分析,金属与酸反应金属溶于酸而使溶液质量增加,金属与盐溶液反应溶液质量的变化取决于参加反应的金属的质量和反应后置换出的金属的质量,若参加反应的金属的质量大于生成的金属或气体的质量,则溶液质量增加,据此分析问题即可.
解答:解:A、铁与稀盐酸能反应,生成氢气和氯化亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+H2SO4═FeSO4+H2↑,可知56gFe反应溶液增加(56-2)=54g,溶液质量增加,故A符合题意;
B、铁的金属活动性比铜强,所以铁与AgNO3反应生产硝酸亚铁和银,
Fe+CuSO4═FeSO4+Cu
56 64
参加反应的铁的质量小于生成的铜的质量,所以溶液质量减小,故B不符合要求;
C、铁与硫酸锌接触时,由于铁的活动性比锌弱,所以两者不会反应,溶液质量不会变化,故C不符合题意;
D、铁的金属活动性比银强,所以铁与硫酸铜反应生产硫酸亚铁和铜,
Fe+2AgNO3═2Ag+Fe(NO3)2
56 216
参加反应的铁的质量小于生成的银的质量,所以溶液质量减小,故D不符合题意;
故选A.
B、铁的金属活动性比铜强,所以铁与AgNO3反应生产硝酸亚铁和银,
Fe+CuSO4═FeSO4+Cu
56 64
参加反应的铁的质量小于生成的铜的质量,所以溶液质量减小,故B不符合要求;
C、铁与硫酸锌接触时,由于铁的活动性比锌弱,所以两者不会反应,溶液质量不会变化,故C不符合题意;
D、铁的金属活动性比银强,所以铁与硫酸铜反应生产硫酸亚铁和铜,
Fe+2AgNO3═2Ag+Fe(NO3)2
56 216
参加反应的铁的质量小于生成的银的质量,所以溶液质量减小,故D不符合题意;
故选A.
点评:本题考查了金属与酸或盐反应时溶液质量的变化,完成此题,可以依据物质间反应的化学方程式进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
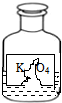 (2010?平南县二模)对如图有污损标签的试剂的猜测与检验方法,不合理的是( )
(2010?平南县二模)对如图有污损标签的试剂的猜测与检验方法,不合理的是( )