题目内容
在潜水艇中常用过氧化钠( Na2O2)来吸收官兵呼出的二氧化碳气体,并产生氧气,供给人的呼吸,其反应的化学方程式为:2 Na2O2+2CO2= 2Na2CO3+O2↑。现有975g过氧化钠样品与足量的二氧化碳反应,可生成160g氧气。试计算样品中含过氧化钠的质量分数。
解:设样品中含过氧化钠的质量为x,则:
2Na2O2+2CO2=2Na2CO3 +O2↑
156 32
x 160 g
 ,解得x=780g
,解得x=780g
样品中过氧化钠的质量分数: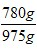 ×100%= 80%
×100%= 80%
2Na2O2+2CO2=2Na2CO3 +O2↑
156 32
x 160 g
 ,解得x=780g
,解得x=780g 样品中过氧化钠的质量分数:
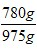 ×100%= 80%
×100%= 80%
练习册系列答案
相关题目