题目内容
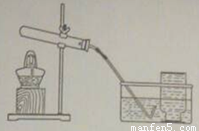
某同学在实验室用木炭和氧化铜的混合物18g用酒精喷灯加热一段时间,冷却后称量固体剩余物为13.6g.请按要求完成下列问题:
(1)写出反应的化学方程式 ;
(2)根据质量守恒定律计算产生的气体的质量为 ;
(3)根据化学方程式计算:剩余固体中含有铜的质量是多少?(要有完整的计算步骤)
(1)写出反应的化学方程式
(2)根据质量守恒定律计算产生的气体的质量为
(3)根据化学方程式计算:剩余固体中含有铜的质量是多少?(要有完整的计算步骤)
分析:因为碳完全反应所以反应前后固体的质量之差即为碳与氧化铜反应生成的二氧化碳质量,利用该值即可依据方程式求出生成物中铜的质量.
解答:解:(1)依据碳与氧化铜的反应可书写出相关的方程式:C+2CuO
CO2↑+2Cu;
(2)依据质量守恒定律可知生成CO2的质量为18g-13.6g=4.4g;
(3)设生成铜的质量为x
C+2CuO
CO2↑+2Cu
44 128
4.4g x
=
x=12.8g
故答案为:(1)C+2CuO
CO2↑+2Cu;(2)4.4g;(3)剩余固体中含有铜的质量是12.8g;
| ||
(2)依据质量守恒定律可知生成CO2的质量为18g-13.6g=4.4g;
(3)设生成铜的质量为x
C+2CuO
| ||
44 128
4.4g x
| 44 |
| 4.4g |
| 128 |
| x |
x=12.8g
故答案为:(1)C+2CuO
| ||
点评:此题是对化学方程式计算的考查题,解题的关键是掌握固体的质量变化即是生成的二氧化碳的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (2013?广州)某同学在实验室用以下装置制备氧气并探究氧气的性质.
(2013?广州)某同学在实验室用以下装置制备氧气并探究氧气的性质.