题目内容
【题目】随着经济的发展,能源与环境成为人们日益关注的问题。
(1)煤、______和________常称为三大化石燃料。
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是_________。
(3)为减少环境污染,科学家致力于研究将二氧化氮和一氧化碳在催化剂和加热的条件下反应,转化为氮气和二氧化碳。该反应的化学方程式为:__________。
(4)“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物。其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是_______(填字母序号,下同)。
A甲醇(CH4O) B甲酸(CH2O2) C乙醇(C2H6O) D乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是_______。
A大量使用化石燃料
B植树造林,增大植被面积
C将二氧化碳变废为宝,循环利用
【答案】石油 天然气 增大煤与氧气的接触面积,促进燃烧 ![]() B BC
B BC
【解析】
(1)煤、石油和天然气是常规的化学燃料;
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是增大煤与氧气的接触面积,促进燃烧;
(3)根据题意得该反应的反应物是二氧化氮和一氧化碳,生成物是氮气和二氧化碳,反应条件是加热和催化剂,所以该反应的化学方程式为:![]() ;
;
(4)根据题意得要想实现零排放则需要满足碳氧原子的个数比为1:2,选项中只有B选项符合题意;
(5)大量使用化石燃料不会减少二氧化碳的排放,反而会增加二氧化碳的排放,不符合题意;植树造林,增大植被面积可以增加二氧化碳的吸收量,减少空气中的二氧化碳;将二氧化碳变废为宝,可以减少二氧化碳的排放。故选BC。

【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为_______________g;
(2)原混合物中氯酸钾的质量是多少?_____________
【题目】下列归纳总结完全正确的一组是()
A 分子特征 | B 数字含义 |
①水分子很小 ②固体物质的分子不运动 ③气体分子间的间隔很大 | ① ② ③NO2 :1个二氧化氮分子中含有2个原子 |
C 实验安全 | D 常见物质 |
①把鼻孔凑到容器口闻药品 ②不能用手接触药品 ③不能尝任何药品的味道 | ①区分氯酸钾和高锰酸钾:观察颜色 ②区分硬水和软水:加肥皂水后搅拌 ③区分过氧化氢溶液和水:加入MnO2观察现象 |
A.AB.BC.CD.D
【题目】水是生命之源,人类的日常生活离不开水。
(1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,净化程度相对较高的是________。
(2)写出电解水的化学反应方程式:________;该反应的基本类型是________________。
(3)A、B、C三种固体的溶解度曲线如下图所示:
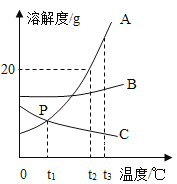
①P点的含义是________;
②t2℃时,将15gA物质加入50g水中,充分溶解后,形成溶液的质量为________g;
③若A物质中含有少量的B物质,提纯A物质的方法是________(填“降温”或“蒸发”)结晶。
(4)下表是![]() 在水中的溶解度的几组数据:(单位:mL)
在水中的溶解度的几组数据:(单位:mL)
温度/t℃ | 0 | 25 | 50 | 75 | 100 |
压强101KPa 1时的溶解度 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
压强101KPa 10时的溶解度 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
压强101KPa 25时的溶解度 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
①根据数据![]() 在水中的溶解度随温度的升高而________(填“增大”或“减小”)。
在水中的溶解度随温度的升高而________(填“增大”或“减小”)。
②打开汽水瓶盖有气体溢出,说明原瓶内的气压________(填“>”“=”或“<”)瓶外大气压。
(5)配制500克溶质质量分数为0.9%的生理盐水,正确的实验操作顺序是________(填序号)
①溶解 ②溶液装瓶、贴标签 ③称量 ④计算 ⑤量取