题目内容
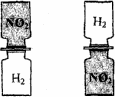
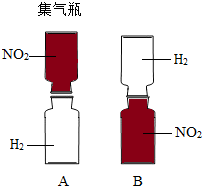
把分别充满红棕色二氧化氮(NO2)气体和氢气的集气瓶按如图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需要很长时间才能达到同样的效果.由此现象不能得出的结论是( )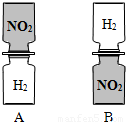
A.分子由原子构成
B.分子间有间隔
C.二氧化氮的密度比氢气大
D.分子是不断运动的
【答案】分析:因为氢气分子和二氧化氮分子在不断运动,且分子间有间隔,氢气的密度小,向上运动,二氧化氮的密度大,向下运动,所以A瓶中的颜色很快趋于一致,B瓶中的混合较慢是因为氢气密度小,在上面运动,二氧化氮密度大,在下面运动的原因
解答:解:A、A中两瓶气体的颜色很快趋于一致,说明分子在不断运动,有的二氧化氮分子运动到有的氢分子之间的间隔中去了,有的氢分子运动到有的二氧化氮分子之间间隔中去了,说明分子之间有间隔,由A中两瓶气体的颜色很快趋于一致,B中需要很长时间才能达到同样的效果,可知氢气的密度小于二氧化氮的密度,由上边的现象不能说明分子由原子构成,故A不能得出结论;
B、两种气体能混合,说明分子间有间隔,故B能得出结论.
C、A瓶混合较快,B瓶混合较慢,说明氢气的密度比二氧化氮密度小,故C能得出结论;
D、此现象能直接得出分子在不断运动的结论,故D能得出结论;
故选A.
点评:此实验能从多角度证明分子的性质,是一个很有代表性的实验.
解答:解:A、A中两瓶气体的颜色很快趋于一致,说明分子在不断运动,有的二氧化氮分子运动到有的氢分子之间的间隔中去了,有的氢分子运动到有的二氧化氮分子之间间隔中去了,说明分子之间有间隔,由A中两瓶气体的颜色很快趋于一致,B中需要很长时间才能达到同样的效果,可知氢气的密度小于二氧化氮的密度,由上边的现象不能说明分子由原子构成,故A不能得出结论;
B、两种气体能混合,说明分子间有间隔,故B能得出结论.
C、A瓶混合较快,B瓶混合较慢,说明氢气的密度比二氧化氮密度小,故C能得出结论;
D、此现象能直接得出分子在不断运动的结论,故D能得出结论;
故选A.
点评:此实验能从多角度证明分子的性质,是一个很有代表性的实验.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
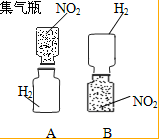 26、如图所示,把充满红棕色二氧化氮气体和无色氢气的集气瓶中间的玻璃片抽走,使两瓶口紧密合在一起(不要振荡),可观察到A中两瓶气体的颜色很快趋于一致(两种气体不反应),而B中需很长时间才能达到同样的效果.观察、对比试验现象,你能得出的结论有:
26、如图所示,把充满红棕色二氧化氮气体和无色氢气的集气瓶中间的玻璃片抽走,使两瓶口紧密合在一起(不要振荡),可观察到A中两瓶气体的颜色很快趋于一致(两种气体不反应),而B中需很长时间才能达到同样的效果.观察、对比试验现象,你能得出的结论有: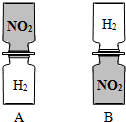 把分别充满红棕色二氧化氮(NO2)气体和氢气的集气瓶按如图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需要很长时间才能达到同样的效果.由此现象不能得出的结论是( )
把分别充满红棕色二氧化氮(NO2)气体和氢气的集气瓶按如图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需要很长时间才能达到同样的效果.由此现象不能得出的结论是( )