题目内容
(1)某品牌补钙药品的部分说明书如图1所示.
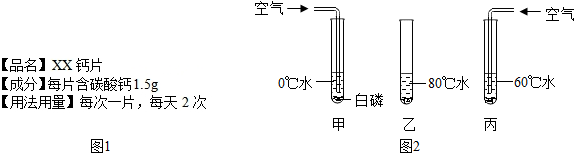
若人体对该药品中钙的平均吸收率为30%,按照说明书服用,每天实际被人体吸收的钙元素质量为 .
(2)甲、乙、丙三个试管分别注入同体积不同温度的水,分别放入相同质量的白磷(着火点为40℃)如图2所示:问写出白磷燃烧的化学方程式 . 试管内白磷不燃烧,其原因分别是
. 试管丙内白磷能否燃烧 ,其原因是 .

若人体对该药品中钙的平均吸收率为30%,按照说明书服用,每天实际被人体吸收的钙元素质量为
(2)甲、乙、丙三个试管分别注入同体积不同温度的水,分别放入相同质量的白磷(着火点为40℃)如图2所示:问写出白磷燃烧的化学方程式
考点:化合物中某元素的质量计算,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:实验性简答题,化学式的计算
分析:(1)由题意,每片含1.5gCaCO3,每次一片,每天2次,由化合物中某元素的质量=该化合物的质量×该元素的质量分数,若人体对该药品中钙的平均吸收率为30%,据此进行分析解答.
(2)根据磷燃烧的原理和可燃物燃烧的条件来分析.
(2)根据磷燃烧的原理和可燃物燃烧的条件来分析.
解答:解:(1)由题意,每片含1.5gCaCO3,每次一片,每天2次,则每天服用的碳酸钙的质量为:1.5g×2=3g,其中含钙元素的质量为3g×
×100%=1.2g;若人体对该药品中钙的平均吸收率为30%,则按照说明书服用,每天实际被人体吸收的钙元素质量是1.2g×30%=0.36g.
故答案为:0.36g.
(2)白磷燃烧生成五氧化二磷;可燃物只有在温度达到其着火点以及与氧气接触的条件下才能发生燃烧.甲试管中的白磷温度没有达到其着火点,不能燃烧;乙试管中的白磷没有与氧气接触,也不能燃烧;丙试管中的白磷既与氧气接触,温度又达到了其着火点,故能发生燃烧.故填:4P+5O2
2P2O5;甲、乙;温度没有达到白磷的着火点;没有与氧气接触;能;既与氧气接触,温度又达到了其着火点.
| 40 |
| 40+12+16×3 |
故答案为:0.36g.
(2)白磷燃烧生成五氧化二磷;可燃物只有在温度达到其着火点以及与氧气接触的条件下才能发生燃烧.甲试管中的白磷温度没有达到其着火点,不能燃烧;乙试管中的白磷没有与氧气接触,也不能燃烧;丙试管中的白磷既与氧气接触,温度又达到了其着火点,故能发生燃烧.故填:4P+5O2
| ||
点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.物质燃烧的条件是中考中经常考查的问题之一,需要同学们能够重点掌握.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
某化学反应的微观模拟示意图如图,从图中获得的有关信息不正确的是( )
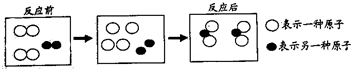

| A、反应前物质的组成属于混合物 |
| B、反应前后分子种类没有发生改变 |
| C、该反应的本质是原子的重新组合 |
| D、该化学反应属于化合反应 |
某同学量取液体时仰视读出体积为12mL,则倒出的液体为( )
| A、>12 mL |
| B、<12 mL |
| C、=12 mL |
| D、无法判断 |
下列变化属于化学变化的是( )
| A、汽油挥发 | B、水结成冰 |
| C、电灯发光 | D、面包发霉 |
下列实验方案中,能达到预期目的是( )
| A、用澄清石灰水除去一氧化碳中混有少量的二氧化碳 |
| B、用大理石和稀硫酸制取二氧化碳 |
| C、用点燃法除去二氧化碳中含有少量的一氧化碳 |
| D、用向下排空法收集CO |
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.