题目内容
【题目】某化工厂用废硫酸制备硫酸钾的流程如下,请回答下列问题:
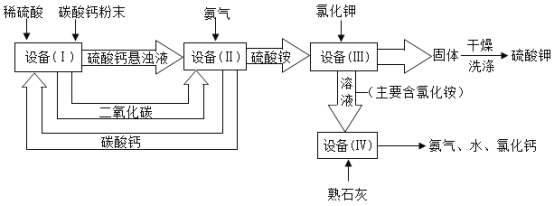
(1)“设备Ⅰ”中将碳酸钙研成粉末的目的是_____________________。
(2)写出“设备Ⅱ”中有关反应的化学方程式____________________。
(3)若在化学实验室分离“设备Ⅲ”中的混合物,用到的操作名称是______________。
(4)上述流程中可循环使用的物质除水外,还有_________________________(填写化学式)。
【答案】增大反应物接触面积,使反应充分,加快反应的速率 CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4 过滤 CaCO3和NH3
【解析】
(1)将碳酸钙研成粉末可以增大碳酸钙与其它反应物的接触面积,使反应充分反应,进而加快反应的速率,故填增大反应物的接触面积,使反应充分,加快反应的速率。
(2)由图可知,设备Ⅱ中的反应是硫酸钙、二氧化碳、氨气和水反应生成碳酸钙沉淀和硫酸铵,故反应的化学方程式写为:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4。
(3)“设备Ⅲ”中的混合物是由固体与液体组成的,分离不溶性固体与液体组成的混合物的操作是过滤,故填过滤。
(4)由图可知,流程中可循环使用的物质除水外,还有设备II中生成的碳酸钙和设备IV生成的氨气,其化学式分别是CaCO3、NH3,故填CaCO3和NH3。

练习册系列答案
相关题目