题目内容
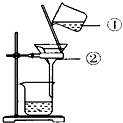
【题目】某山区所饮用的水常是河水,由于河水中常含有大量的泥沙、悬浮物和细菌等杂质,可用次氯酸(HClO)杀死细菌,将漂白粉(主要成分是Ca(ClO)2)溶于水可生成可溶性氯化钙和次氯酸.下列是某户居民在饮用水之前对河水的处理步骤:
河水→A(明矾)→B(沉淀)→C(过滤)→D(活性炭)→E(漂白粉)→净水
(1)其中发生化学变化的步骤为 . (填编号)
(2)A步中加明矾的作用是 .
(3)下列是一些净水的方法,其中可使硬水变成软水的是:(填序号).
①过滤②蒸馏③沉淀④煮沸
(4)按如图所示装置进行实验,一般时间后,理论上A试管中产生的气体与B试管中产生的气体的体积比为 , 该实验过程中发生反应的文字表达式为 . 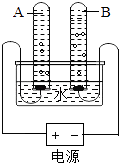
(5)检验A试管的气体常用 .
【答案】
(1)E
(2)吸附悬浮杂质,加速沉降
(3)②④
(4)1:2;水 ![]() 氢气+氧气
氢气+氧气
(5)带火星的木条,能使带火星的木条复燃
【解析】解:(1)加入漂白粉时有新物质生成,发生的是化学变化;(2)由于明矾溶于水的生成物具有吸附性,所以加入明矾的作用是吸附悬浮杂质,加速沉降;(3)在净化水时,煮沸和蒸馏都能除去水钙、镁离子的化合物,能降低水的硬度;(4)按如图所示装置进行实验,一般时间后,A试管中产生的气体是电源的正极产生的气体是氧气,B试管中产生的气体是电源的负极产生的气体是氢气,理论上体积比为1:2,该实验过程中发生反应的文字表达式为:水 ![]() 氢气+氧气.(5)由上述分析可知,A试管的气体是氧气具有助燃性,检验A试管的气体常用带火星的木条,能使带火星的木条复燃.故答为:(1)E;(2)吸附悬浮杂质,加速沉降(3)②④(4)1:2;水
氢气+氧气.(5)由上述分析可知,A试管的气体是氧气具有助燃性,检验A试管的气体常用带火星的木条,能使带火星的木条复燃.故答为:(1)E;(2)吸附悬浮杂质,加速沉降(3)②④(4)1:2;水 ![]() 氢气+氧气(5)带火星的木条,能使带火星的木条复燃.
氢气+氧气(5)带火星的木条,能使带火星的木条复燃.
【考点精析】本题主要考查了电解水实验和水的净化的相关知识点,需要掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑;水的净化效果由低到高的是静置、吸附、过滤、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭才能正确解答此题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案