题目内容
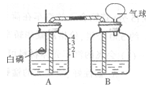
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究。
【推理假设】上述两种物质发生反应的化学方程式为: ,由此
推测出废液中一定有NaCl,可能有Na2CO3或盐酸。
【实验探究】(1)确定废液中是否含有盐酸:
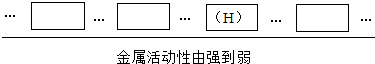
①选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质X是酸碱指示剂中的 溶液。
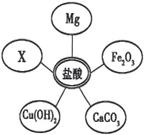
②实验验证:某同学向废液中加入少量的镁粉,观察到 ,确定废液中一定没有盐酸。
(2)确定废液中是否含有Na2CO3:某同学选用 测出废液的pH=l0,确定废液中一定含有Na2CO3。
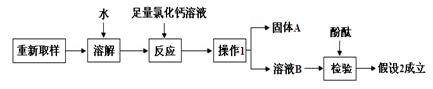
(3)处理废液,回收利用:欲从废液中得到纯净的NaCl,请完成如下实验方案设计。
(4)拓展运用:
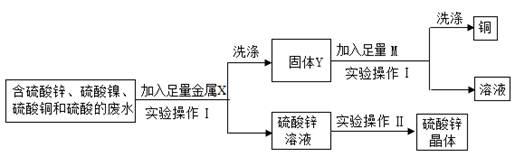
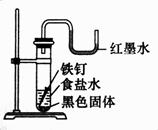
按如下图方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是 。
【推理假设】上述两种物质发生反应的化学方程式为: ,由此
推测出废液中一定有NaCl,可能有Na2CO3或盐酸。
【实验探究】(1)确定废液中是否含有盐酸:
①选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质X是酸碱指示剂中的 溶液。

②实验验证:某同学向废液中加入少量的镁粉,观察到 ,确定废液中一定没有盐酸。
(2)确定废液中是否含有Na2CO3:某同学选用 测出废液的pH=l0,确定废液中一定含有Na2CO3。
(3)处理废液,回收利用:欲从废液中得到纯净的NaCl,请完成如下实验方案设计。
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行,理由是: |
| 二 | 稍过量的 | | 可行 |
(4)拓展运用:
按如下图方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是 。

【推理假设】 Na2CO3+2HCl=2Na Cl+ H2O+ CO2↑。
【实验探究】(1)①石蕊试液 ②无明显现象 (2)pH试纸。
(3)不可行,理由是:氯化钠中混有硝酸钠杂质。
实验方案设计:加入试剂:稀盐酸,分离方法:蒸发结晶。
(4)拓展运用:溶质是Na2CO3。
【实验探究】(1)①石蕊试液 ②无明显现象 (2)pH试纸。
(3)不可行,理由是:氯化钠中混有硝酸钠杂质。
实验方案设计:加入试剂:稀盐酸,分离方法:蒸发结晶。
(4)拓展运用:溶质是Na2CO3。
试题分析:【推理假设】根据碳酸钠与盐酸反应的实质写出其反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;【实验探究】(1)①判定废液中是否含盐酸所取用的酸碱指示剂不能用酚酞试剂,因酸不能使无色的酚酞变色,故取用紫色石蕊试液,酸能使紫色石蕊试液变红色;②镁和盐酸反应出现的现象是产生大量气泡,如没气泡产生则证明废液中一定没有盐酸;(2)测定溶液的酸碱性的最简单方法用pH试纸;(3)根据化学上除杂质原则分析实验方案设计,即除去原杂质不能添加新的杂质,因而处理废液,回收利用废液中得到纯净的NaCl时,如加适量Ca(NO3)2溶液,虽然除去了碳酸钠,但却引进新杂质NaNO3;如加入过量的稀盐酸蒸发结晶后可得到纯净的氯化钠.(4)根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.分离BaCl2和NaCl的固体混合物时,X溶液中溶质是Na2CO3。

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目