题目内容
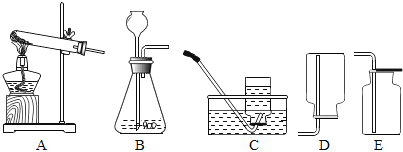
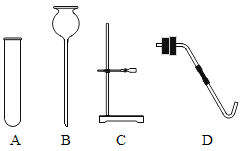
【题目】请根据下列所示实验装置图回答问题:

(1)写出B装置图中仪器的名称:_____、_____。
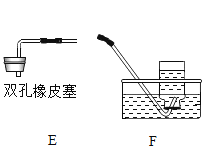
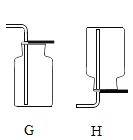
(2)若A、F组成制取某气体M的装置,制取此气体的化学方程式为_____;用B装置也可制取M气体,发生装置中的化学反应方程式是_____。
(3)将浓盐酸和大理石在B装置中混合后发生剧烈反应,此反应的化学方程式是_____,但把生成的气体直接通入澄清石灰水时,石灰水没有变浑浊。你认为石灰水没有变浑浊的原因是_____。
(4)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取少量氨气(NH3),同时得到氯化钙和水。
①该反应应当在_____装置内进行,其发生反应的化学方程式是_____。
②收集氨气时应选用E装置,当把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量红色液体进入。据此推测氨气的性质是_____。
【答案】锥形瓶 长颈漏斗 2KClO3![]() 2KCl+3O2↑ 2H2O2
2KCl+3O2↑ 2H2O2![]() 2H2O+O2↑ CaCO3+2HCl =CaCl2+H2O+CO2↑ 浓盐酸具有强烈的挥发性,使制得的二氧化碳气体中混有氯化氢气体,与氢氧化钙发生了反应 A 2NH4Cl+Ca(OH)2
2H2O+O2↑ CaCO3+2HCl =CaCl2+H2O+CO2↑ 浓盐酸具有强烈的挥发性,使制得的二氧化碳气体中混有氯化氢气体,与氢氧化钙发生了反应 A 2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O 氨气的密度比空气小、氨气易溶于水、氨气的水溶液呈碱性
2NH3↑+CaCl2+2H2O 氨气的密度比空气小、氨气易溶于水、氨气的水溶液呈碱性
【解析】
(1)B装置中的仪器有锥形瓶、长颈漏斗。
(2)用A、F组成制取某气体,是固体加热型反应,气体不易溶于水,则可以是加热氯酸钾和二氧化锰的混合物制取氧气,用C装置也可制取氧气,则是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,故填:2KClO3![]() 2KCl+3O2↑;2H2O2
2KCl+3O2↑;2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(3)碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,反应的方程式为:CaCO3+2HCl =CaCl2+H2O+CO2↑;浓盐酸具有强烈的挥发性,使制得的二氧化碳气体中混有氯化氢气体,与氢氧化钙发生了反应。
(4)①加热氯化铵和氢氧化钙固体混合物的方法制取少量氨气(NH3)属于固固加热型装置,故该反应在A装置中进行。氯化铵和氢氧化钙固体混合物加热生成氨气和氯化钙和水,该反应的方程式为:2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;
2NH3↑+CaCl2+2H2O;
②收集氨气时应选用向下排空气法(E装置)可知氨气的密度比空气小;把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量液体进入说明氨气极溶于水;溶液变成红色(无色酚酞溶液遇碱变红),说明氨气的水溶液呈碱性;故答案为:氨气的密度比空气小、氨气易溶于水、氨气的水溶液呈碱性。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
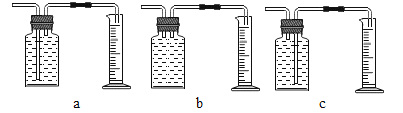
小学生10分钟应用题系列答案【题目】某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
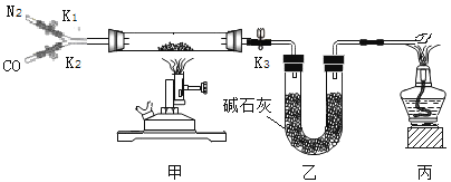
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤II硬质玻璃 管和剩余固体 | 步骤步骤Ⅲ硬质玻璃 管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2-m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3-m4
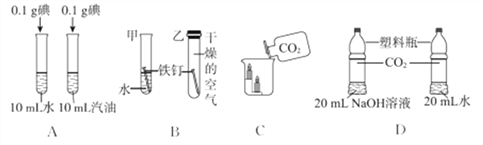
【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究 CO2 通入NaOH 溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验序号 | 实验步骤一 | 实验步骤二 | 实验序号 | 实验步骤一 | 实验步骤二 |
实验 I |
|
| 实验II |
|
|
(探究与结论)
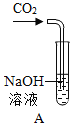
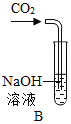
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是_____。
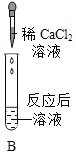
(2)实验Ⅱ中步骤二发生的化学方程式是_____,其中CaCl2溶液也可以用_____(填字母)代替达到实验目的。
A 硝酸钡溶液 B 氯化钾溶液 C 碳酸钾溶液 D 硫酸钠溶液
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是_____。
(拓展延伸)现有下列信息:

请你和化学兴趣小组的同学一起利用以上资料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:_____。看到的现象是_____。