题目内容
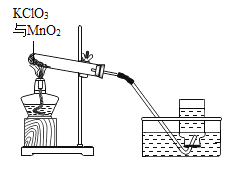
【题目】某化学兴趣小组用下图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。
加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 3.0 | 2.25 | 2.04 | 2.04 |
(1)当反应完全后,共制得氧气_____g。
(2)制取结束后,将剩余固体用适量水充分溶解,采取_____的方法,以回收MnO2,再烘干称量MnO2其质量为_____g(不计过程中的损失)。
(3)计算原混合物中氯酸钾的质量分数是多少?_____(精确到0.1%)
【答案】0.96g 过滤 0.55g 81.7%
【解析】
根据反应原理,固体减少的质量就是生成氧气的质量,依据表格数据,求出氧气的质量,再用氧气的质量求出氯酸钾的质量和二氧化锰的质量,以及混合物中氯酸钾的质量分数。
(1)根据质量守恒定律,当反应完全后,共制得氧气的质量为![]() 。
。
(2)制取结束后,剩余固体为氯化钾和二氧化锰,氯化钾能溶于水,二氧化锰难溶于水,用适量水充分溶解剩余固体,采取过滤的方法,可以回收MnO2,再烘干称量。
设氯酸钾的质量为X。
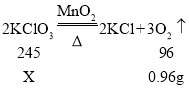
![]()
![]()
那么,二氧化锰的质量为![]() 。
。
(3)原混合物中氯酸钾的质量分数为![]() ;
;
答:原混合物中氯酸钾的质量分数81.7%。

练习册系列答案
相关题目