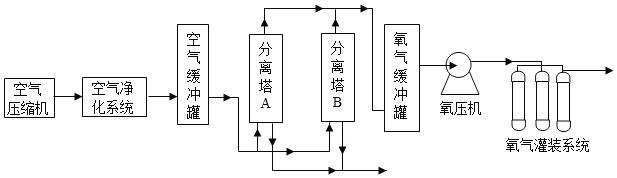
题目内容
【题目】根据下列五种微粒的结构示意图,回答下列问题:
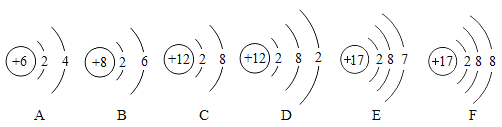
(1)在以上粒子中,属于同种元素的是___和___、___和___;属于原子的有_____,属于阳离子的有___
(2)写出以上粒子能形成的化合物的化学式___
(3)B在化学反应中,易____电子变成____(填“阴”或“阳”)离子
(4)最外层电子层达到稳定结构的是 ______
【答案】C D E F ABDE C CO2 、MgO 、MgCl2等 得 阴 CF
【解析】
本题主要考察原子结构示意的相关知识
(1)质子数相同属于同种元素,C和D ,E和F;质子数=核外电子数的微粒属于原子,A是碳原子,B是氧原子,D镁原子,E氯原子,原子失电子形成阳离子,C是Mg2+
(2)图中共有碳、氧、镁、氯元素,可以形成的化合物有CO2 、MgO 、MgCl2等
(3)B是氧原子,最外层电子数是6,容易得电子,形成阴离子
(4)最外层8个电子稳定的有C和F

练习册系列答案
相关题目
【题目】下列说法完全正确的是( )
A | 氖气的化学式—— 1个硅原子—— 1个钠离子--- | B | 决定元素种类——质子数 决定元素化学性质——最外层电子数 决定元素在周期表中的周期序数——电子层数 |
C | 铁——由分子构成 二氧化碳——由原子构成 硫酸铜——由离子构成 | D | 分子——化学变化中的最小粒子 原子——保持物质化学性质的最小粒子 离子——带电的原子或原子团 |
A. AB. BC. CD. D
【题目】用如图所示装置探究燃烧的条件。(提示,白磷的着火点为40oC)
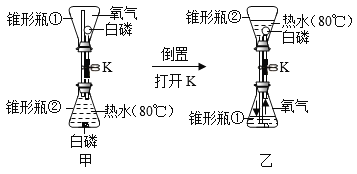
(1)通过下表进行现象分析:____________
可燃物 | 与氧气接触 | 温度达到着火点 | 是否燃烧 | |
甲① | ||||
甲② | ||||
乙①(例) | √ | ╳ | √ | ╳ |
乙② |
(2)通过以上分析,推出燃烧需要氧气的依据是____________。