题目内容
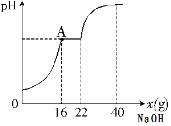
【题目】整理实验室时,同学们发现一瓶盐酸呈黄色,老师解释说里面含有氯化铁。为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小明做了如下实验:取20g工业盐酸加适量的水稀释后加入小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时不断测量溶液的pH,得出如图所示的关系(横坐标x表示滴加氢氧化钠溶液的质量)。则下列分析错误的是
A.工业盐酸呈黄色是因为含有Fe3+
B.点A时溶液中所含溶质是NaCl和FeCl3
C.当16<x≤22时的实验现象是有红褐色沉淀产生
D.当x =22g时,所得沉淀为19.6g
【答案】D
【解析】
试题分析: 在盐酸存在的条件下,不能形成氢氧化铁沉淀,所以只有把盐酸消耗掉之后,才会生成沉淀,从图中可知与OA段表示加氢氧化钠与盐酸反应,水平线部分是表示氢氧化钠与氯化铁反应;A.含Fe3+的溶液是黄色的,工业盐酸呈黄色是因为含有Fe3+,正确;B.点A时表示氢氧化钠与盐酸恰好完全反应,生成NaCl,此时溶液中所含溶质是NaCl和FeCl3,正确;C.当16<x≤22时表示氢氧化钠与氯化铁反应,现象是有红褐色沉淀产生,正确;D.设当x=22g时,所得沉淀质量为x,
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
120 107
22g-16g x
![]() x=5.35g 故选D
x=5.35g 故选D

练习册系列答案
相关题目
【题目】琳琳找到四种不同的固体物质,进行实验,下表记录了各种物质所具有的特征.那么哪种物质的特征更接近有机物 ( )
特性试验 | 物质A | 物质B | 物质C | 物质D |
熔点 | 高 | 低 | 高 | 低 |
是否溶于水 | 可溶 | 不溶 | 不溶 | 可溶 |
高温下 | 稳定 | 分解 | 稳定 | 稳定 |
是否导电 | 导电 | 不导电 | 不导电 | 导电 |
A. 物质A B. 物质B C. 物质C D. 物质D