题目内容
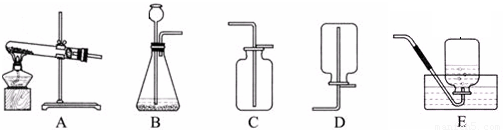
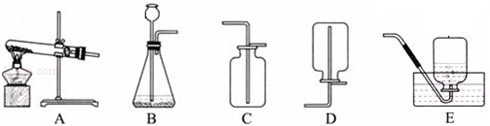
下图是大家所熟悉的实验室制取和收集气体的装置图,请回顾回答以下问题: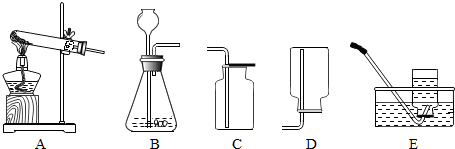
(1)如果要以高锰酸钾为试剂制取一瓶纯净的氧气,应选用
(2)实验室欲制取8.8g二氧化碳,需取用含杂质20%的石灰石
分析:(1)如果要以高锰酸钾为试剂制取一瓶纯净的氧气,分析反应物的状态及反应条件是加热固体制取气体,应选择A装置作发生装置;收集较纯净的气体,应用排水法收集,可用E装置收集,根据反应可以写出方程式;
(2)根据化学方程式计算,由一种生成物的质量,可求反应物的质量,当物质中含有杂质时,应换算成纯净物的质量带入方程式计算;实验室常用稀盐酸和大理石反应制取二氧化碳,是固液反应制取气体,二氧化碳的密度大于空气的密度,应用向上排空法收集二氧化碳气体,可用于制取和收集二氧化碳装置应该选BC.
(2)根据化学方程式计算,由一种生成物的质量,可求反应物的质量,当物质中含有杂质时,应换算成纯净物的质量带入方程式计算;实验室常用稀盐酸和大理石反应制取二氧化碳,是固液反应制取气体,二氧化碳的密度大于空气的密度,应用向上排空法收集二氧化碳气体,可用于制取和收集二氧化碳装置应该选BC.
解答:解:(1)用高锰酸钾制取一瓶纯净的氧气,反应物的状态及反应条件是加热固体制取气体,应选择A装置,收集较纯净的气体,应用排水法收集,可用E装置收集,所以,应选用A E组合装置;反应的方程式是:2KMnO4
K2MnO4+MnO2+O2↑;
(2)设实验室欲制取8.8g二氧化碳,需取用含杂质20%的石灰石的质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x(1-20%) 8.8g
=
x=25g
所以,实验室欲制取8.8g二氧化碳,需取用含杂质20%的石灰石 的质量是25g;
实验室常用稀盐酸和大理石反应制取二氧化碳,是固液反应制取气体,二氧化碳的密度大于空气的密度,应用向上排空法收集二氧化碳气体,可用于其制取和收集二氧化碳装置应该选BC.
故答为:(1)AE,2KMnO4
K2MnO4+MnO2+O2↑;(2)25g,BC.
| ||
(2)设实验室欲制取8.8g二氧化碳,需取用含杂质20%的石灰石的质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x(1-20%) 8.8g
| 100 |
| 44 |
| x(1-20%) |
| 8.8g |
x=25g
所以,实验室欲制取8.8g二氧化碳,需取用含杂质20%的石灰石 的质量是25g;
实验室常用稀盐酸和大理石反应制取二氧化碳,是固液反应制取气体,二氧化碳的密度大于空气的密度,应用向上排空法收集二氧化碳气体,可用于其制取和收集二氧化碳装置应该选BC.
故答为:(1)AE,2KMnO4
| ||
点评:化学是一门以实验为基础的学科,因此实验仪器的使用,装置的选择,实验原理,注意事项,气体的检验,都是中考热点,应加强学习,提高自己的实验技能.

练习册系列答案
相关题目
下图是大家所熟悉的实验室制取和收集气体的装置图,请回顾回答以下问题:
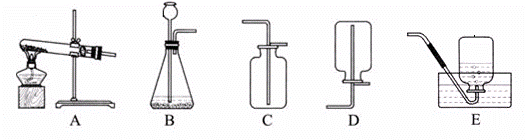 |
(1)如果要以高锰酸钾为试剂制取一瓶纯净的氧气,应选用 (填序号,下同)组合的装置,该反应的化学方程式是__ _ 。
(2)实验室欲制取二氧化碳的反应的化学方程式是 ,
用B装置制取气体时,要求使长颈漏斗的下口深入液面内的目的是 ,
收集二氧化碳只能用装置C的理由是 。
(3)请根据你所掌握的氧气和二氧化碳的制取、收集经验,总结写一条具有可拓展、迁移意义的制取或收集其它气体的规律 。